纸质文物是文化遗产的重要组成部分,记录着大量珍贵的历史资料,如油画、水彩画、书籍、文献、手稿等[1]。据估计,中国古代纸质文物超过3 000万份,其中非常珍贵的文物超过250万份[2]。但纸质文件或纸质艺术品由于其有机成分和吸湿性,易滋生细菌而被降解,最终导致纸张力学性能不可逆的降低[3]。目前所用的抗生素虽有显著的抗菌效果,但其毒副作用、引起的二次感染以及细菌耐药性等问题在一定程度上限制了其应用[4]。因此,研究一种绿色有效的纸张抑菌剂已成为档案馆和博物馆面临的一项具有挑战性的任务[5]。
研究发现,中药可有效解决细菌耐药性问题。小檗碱作为一种传统中药单体[6],其来源丰富,不易产生耐药性,且使用后不会造成二次污染。纤维素是世界上最丰富的天然可再生生物质资源,但其水溶性较差[7]。其衍生物羧甲基纤维素(CMC)具有水溶性、可生物降解、价格低廉;其结构与纸张纤维相似,具有良好的生物相容性;CMC自身羟基可与纸纤维羟基之间键合形成氢键,提高纸张纤维间的键合作用[8]。但CMC有一定的吸水性,可滋生细菌,应用于纸张保护领域受到一定限制。
为保护纸张,解决细菌耐药性问题,本研究在目前国内外纸张抑菌剂研究的基础上,提出了一种新的思路,集盐酸小檗碱(BBR)和CMC两者优点于一体,制备一种具有良好生物相容性,并可生物降解的纸张抑菌剂。其不仅保留了CMC和BBR本身的优点,还赋予纸张良好的抑菌性。该研究为纸质文物的保护提供了一定的理论指导,为小檗碱作为纸质文物抑菌剂提供了参考。
1 试验方案
1.1 试验原材料
金黄色葡萄球菌(S.aureus)、大肠杆菌(E.coli)、黑曲霉(Aspergillus niger)、白念珠菌(Candiada albicans)为本实验室保存菌株;BBR购自国药化学试剂有限公司;CMC购自上海景春生化科技有限公司;氯化钠、氢氧化钾、2,4-二甲氧基苄胺、高碘酸钠购自阿拉丁公司;无水乙醇、无水甲醇、浓盐酸和丙酮购自天津志远化学试剂有限公司;蛋白胨、牛肉膏和琼脂购自北京奥博星生物科技有限责任公司。
1.2 双醛羧甲基纤维素(DCMC)的制备
取1.0 g CMC,20 mL去离子水,于35 ℃、1 500 r/min条件下磁力搅拌12 h。再加入10 mL 0.11 g/mL的NaIO4溶液,用1 mol/L H2SO4将pH值调到3.0,黑暗条件下搅拌4 h,产物用无水乙醇沉淀、洗涤、冻干,得DCMC。
1.3 改性小檗碱的制备
取7.4 g BBR于50 mL三口烧瓶中,再加入15 mL 2,4-二甲氧基苄胺,120 ℃、1 500 r/min搅拌8 h,冷却,用丙酮洗涤,冻干得化合物A。取3 g化合物A溶于甲醇,再加3 mL浓盐酸,室温搅拌6 h,抽滤,用80%乙醇洗涤沉淀,冷冻干燥得改性小檗碱(BBR-NH2)。
1.4 小檗碱化羧甲基纤维素的制备
称取一定量的DCMC和BBR-NH2于三口烧瓶,加入20 mL蒸馏水,在一定温度、pH值、1 500 r/min下搅拌12 h。产物透析、冷冻干燥得小檗碱化羧甲基纤维素(BBR-DCMC)。
1.4.1 单因素实验
取DCMC投量为0.14 g,考察BBR-NH2投量、反应温度和pH值对产物量的影响,对合成工艺进行初步优化,确定各因素较佳范围,每个点测3次,取3次平行实验的均值。
1.4.2 响应面实验设计
取DCMC投量为0.14 g,在单因素实验结果的基础上,选取BBR-NH2投量、反应温度和pH值三因素,利用Box-Benhnken进行三因素三水平的实验设计,因素水平见表1,用软件Design-Expert 8.0 对响应面结果进行分析,寻找合成BBR-DCMC的最适条件。
表1 响应曲面因素水平表
Table 1 Factor level table of response surface

因素水平-101A(反应温度/℃)304050B(反应pH值)456C(BBR-NH2质量/g)0.160.240.32
1.5 产物表征
1.5.1 红外测试
用傅立叶红外光谱仪(型号Nicolet Is5)对CMC、DCMC和BBR-DCMC进行FTIR分析,波谱扫描范围为500~4 000 cm-1。
1.5.2 XRD测试
用型号为D8 Adavance的X射线衍射仪对CMC和BBR-DCMC进行测试。
1.5.3 TG测试
用型号为STA 2500 Regulus的同步热分析仪测试CMC和BBR-DCMC。测试温度为0~800 ℃,升温率10 ℃/min。
1.6 抑菌防霉性能评价
1.6.1 牛肉膏蛋白胨培养基制备
取10.0 g蛋白胨、3.0 g牛肉膏、20.0 g琼脂、5.0 g NaCl于适量蒸馏水中,加热溶解定容至1 000 mL,调pH值为7.2~7.6。分装于锥形瓶高压蒸汽灭菌(120 ℃,30 min)。灭菌完毕,待培养基冷却至45 ℃倒平板(15~20 mL/皿),放冷备用。
1.6.2 最小抑菌浓度(MIC)测定
配制0.1、0.2、0.4、0.6、0.8 mg/mL的5种不同浓度BBR-DCMC的水溶液,将若干直径为6 mm的纸片高压蒸汽灭菌(121 ℃、15 min),晾干后用不同浓度的BBR-DCMC溶液涂覆,取出于无菌室超净工作台上晾干备用。取0.1 mL的1×105 CFU/mL菌悬液于牛肉膏蛋白胨培养基上,均匀涂布,将含药纸片贴平板上,用生理盐水作对照组,后将平板置于恒温培养箱(37 ℃)培养24 h。
2 分析与讨论
2.1 BBR-DCMC的反应机理
BBR-DCMC的反应机理如图1所示。首先,小檗碱C(9)甲氧基脱甲基化形成BBR-NH2[9],CMC被高碘酸钠氧化为DCMC[10](如图1),BBR-NH2的氨基N上孤对电子进攻DCMC上的羰基C,C![]() O中的一个e-给O形成碳四中间体,C原子的双键变成2个单键,一个连接O-,另一个连接—NH2R1基团。随后,O-+H+=—OH,—NH2R1—H+=—NHR1,通过希夫碱反应得到BBR-DCMC[10]。改性羧甲基纤维素具备小檗碱良好的抑菌性,又有CMC抗盐、可再生、可生物降解等特点,其结构类似纸张中的纤维素,与纸张纤维具有良好的生物相容性,提高纤维间的键合作用。将其应用于纸张,可赋予纸张良好的抑菌性能。
O中的一个e-给O形成碳四中间体,C原子的双键变成2个单键,一个连接O-,另一个连接—NH2R1基团。随后,O-+H+=—OH,—NH2R1—H+=—NHR1,通过希夫碱反应得到BBR-DCMC[10]。改性羧甲基纤维素具备小檗碱良好的抑菌性,又有CMC抗盐、可再生、可生物降解等特点,其结构类似纸张中的纤维素,与纸张纤维具有良好的生物相容性,提高纤维间的键合作用。将其应用于纸张,可赋予纸张良好的抑菌性能。
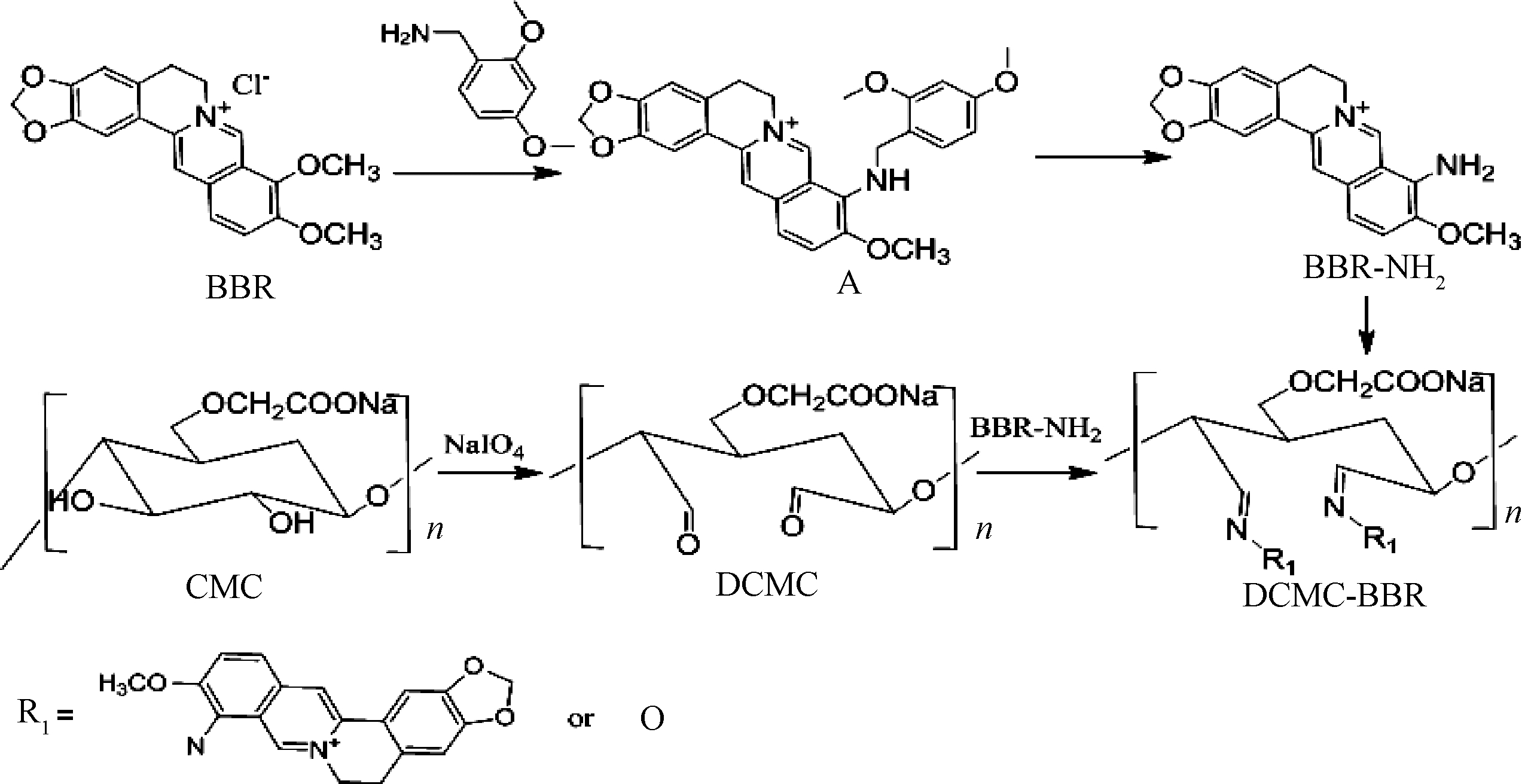
图1 BBR-DCMC的反应机理
Figure 1 Reaction mechanism of BBR-DCMC
2.2 BBR-DCMC的制备
2.2.1 单因素实验
(1)温度对产物量的影响。保持其他条件不变,研究反应温度对产物BBR-DCMC质量的影响,结果如图2所示。
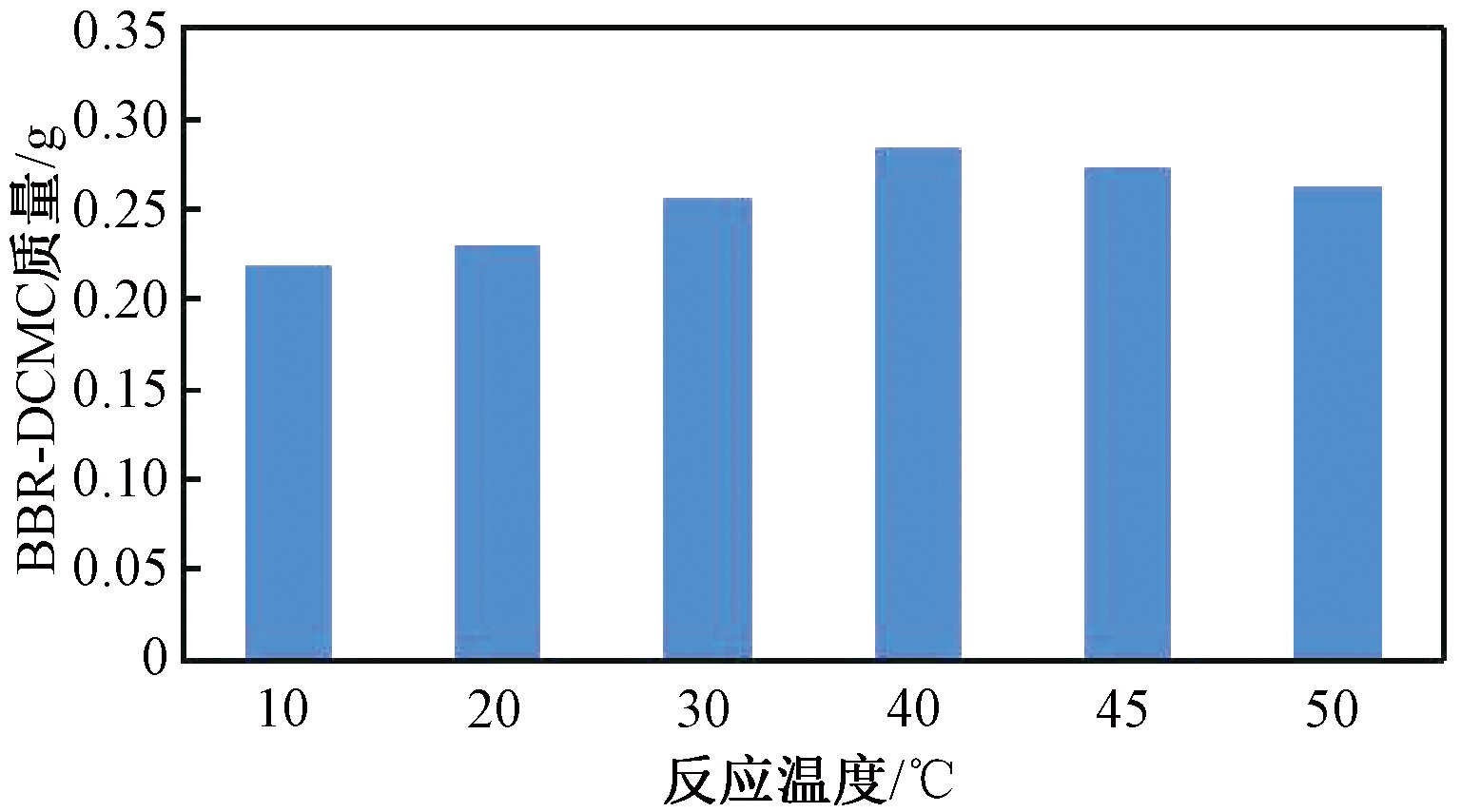
图2 温度对BBR-DCMC的影响
Figure 2 Effect of temperature on BBR-DCMC
如图2所示,随着反应温度的升高,产物BBR-DCMC先增后减。当反应温度较低时,随着温度的升高,分子运动加快,分子之间的有效碰撞概率增加,产物量增加。继续升温,产物量降低,可能是由于DCMC不稳定,使羰基数目变少,产物量降低。当温度达到40 ℃时,产物BBR-DCMC量最高,故反应温度40 ℃为宜。
(2)pH对产物量的影响。保持其他条件不变,研究反应pH对产物BBR-DCMC质量的影响,结果如图3所示。
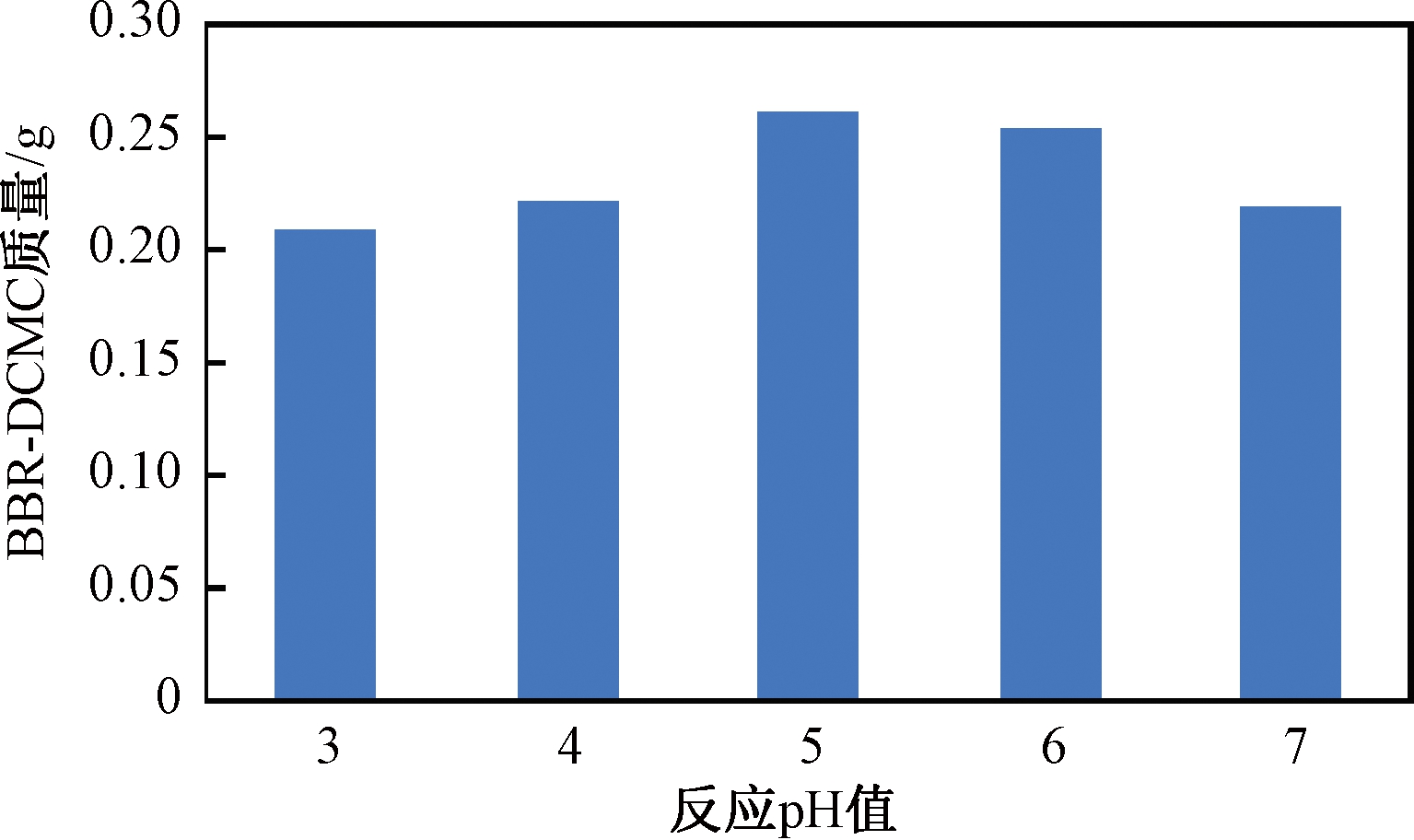
图3 pH对BBR-DCMC的影响
Figure 3 Effect of pH on BBR-DCMC
由图3可知,随着反应体系pH值的增加,产物BBR-DCMC先增后减。当反应体系pH值较低时,可能是BBR-NH2分子中氨基与体系中H+键合作用较强,导致BBR-NH2参与反应的比例减少。继续提高反应体系pH值,产物量降低,可能是BBR-NH2分子中氨基电离出的H+离子与体系中的OH-离子键合,导致参与有效碰撞的BBR-NH2分子比例减少。当pH值为5时,BBR-DCMC的量最高,故反应体系pH值为5为宜。
(3)反应物投料对产物量的影响。保持其他条件不变,研究BBR-NH2的量对BBR-DCMC质量的影响,结果如图4所示。
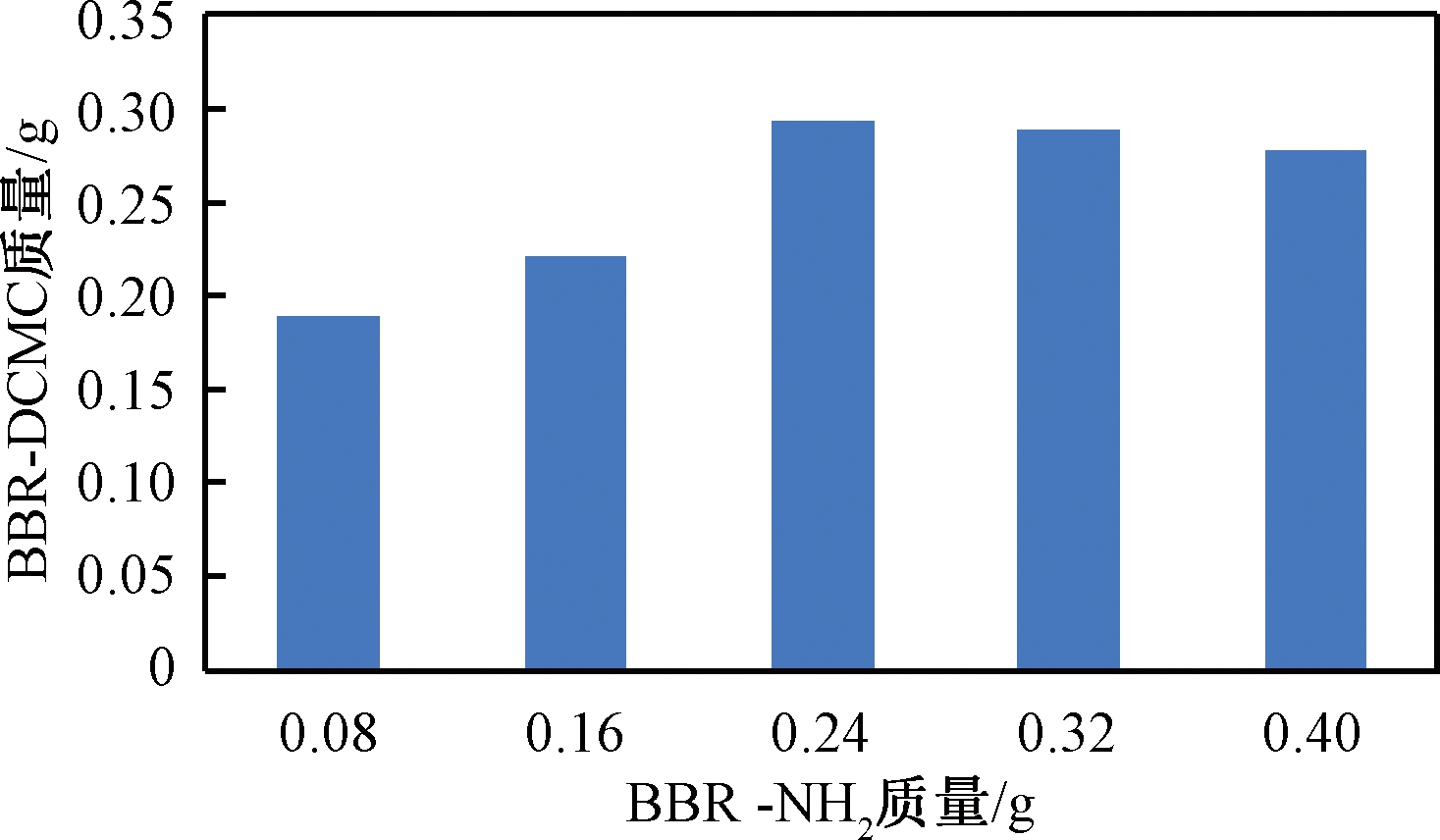
图4 BBR-NH2对BBR-DCMC的影响
Figure 4 Effect of BBR-NH2 on BBR-DCMC
由图4可知,当DCMC量不变,随着BBR-NH2的增加,BBR-DCMC先增后减。当BBR-NH2量较少时,随着BBR-NH2量增加,DCMC和BBR-NH2碰撞概率增大,产物增加。当BBR-NH2质量为0.24 g时,BBR-DCMC达到最大,再继续增加BBR-NH2的量,已参与反应的BBR-NH2因位阻效应,不利于产物生成,同时还增加成本,故BBR-NH2取0.24 g为宜。
2.2.2 响应面优化的条件
(1)响应面实验分析。响应面实验结果见表2,实验回归模型与方差分析如表3所示。
根据表2,以产物BBR-DCMC的质量为指标,对数据进行回归拟合,得到产物BBR-DCMC的二次多元回归方程:Y=0.31-2.650×10-3A-1.350×10-3B +0.030C-9.150×10-3AB-8.150×10-3AC+4.350×10-3BC-0.044A2-0.029B2-0.022C2。
表2 响应面实验及结果
Table 2 Response surface experiments and results
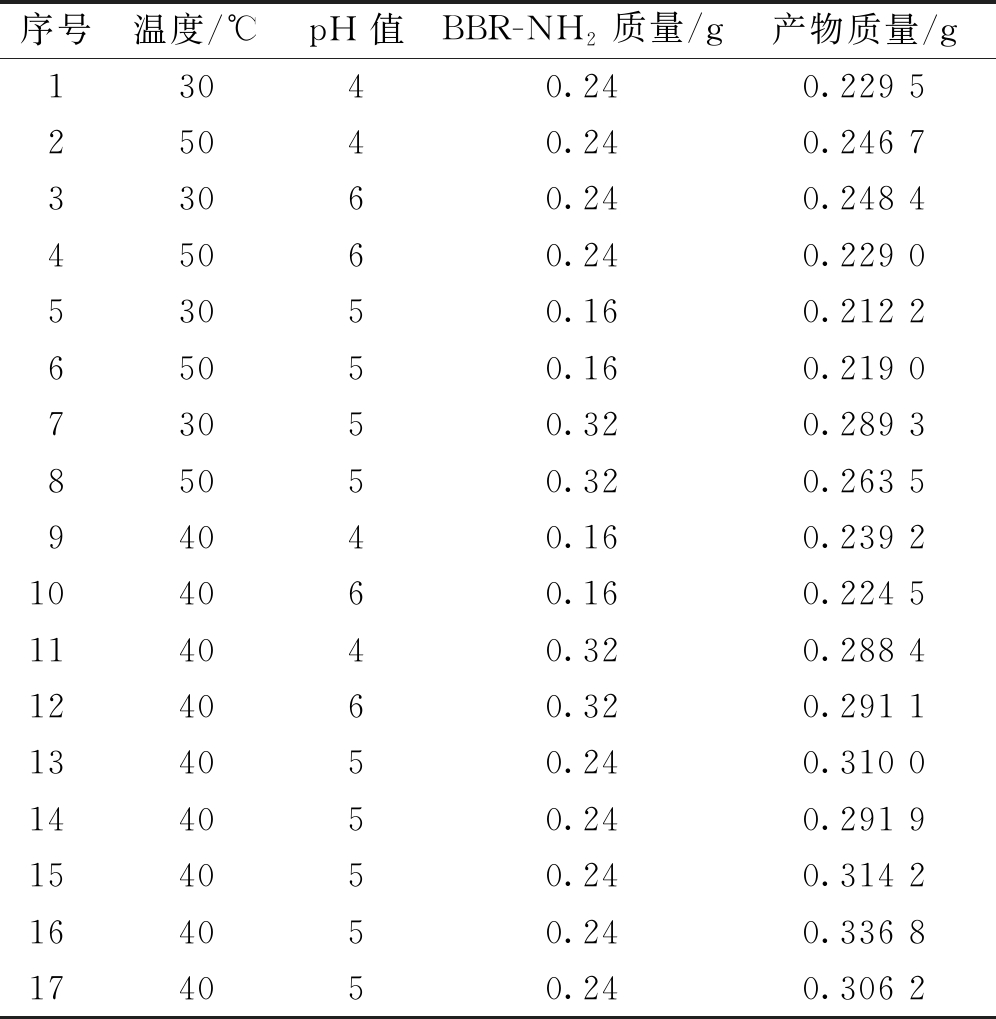
序号温度/℃pH值BBR-NH2质量/g产物质量/g13040.240.229 525040.240.246 733060.240.248 445060.240.229 053050.160.212 265050.160.219 073050.320.289 385050.320.263 594040.160.239 2104060.160.224 5114040.320.288 4124060.320.291 1134050.240.310 0144050.240.291 9154050.240.314 2164050.240.336 8174050.240.306 2
由表3知,三因素对合成BBR-DCMC的影响大小:C(BBR-NH2投量)>A(反应温度)>B(反应pH)。以产物BBR-DCMC建立的回归模型:F=15.95,P=0.000 7<0.001,说明该模型极显著;失拟项F=0.077,P=0.969 2>0.05,即失拟项不显著。说明该模型与实际拟合较好,可靠性强,该多元二次回归方程为分析合成BBR-DCMC提供了较好的模型。
表3 BBR-DCMC合成回归模型与方差分析
Table 3 BBR-DCMC synthetic regression model and variance analysis
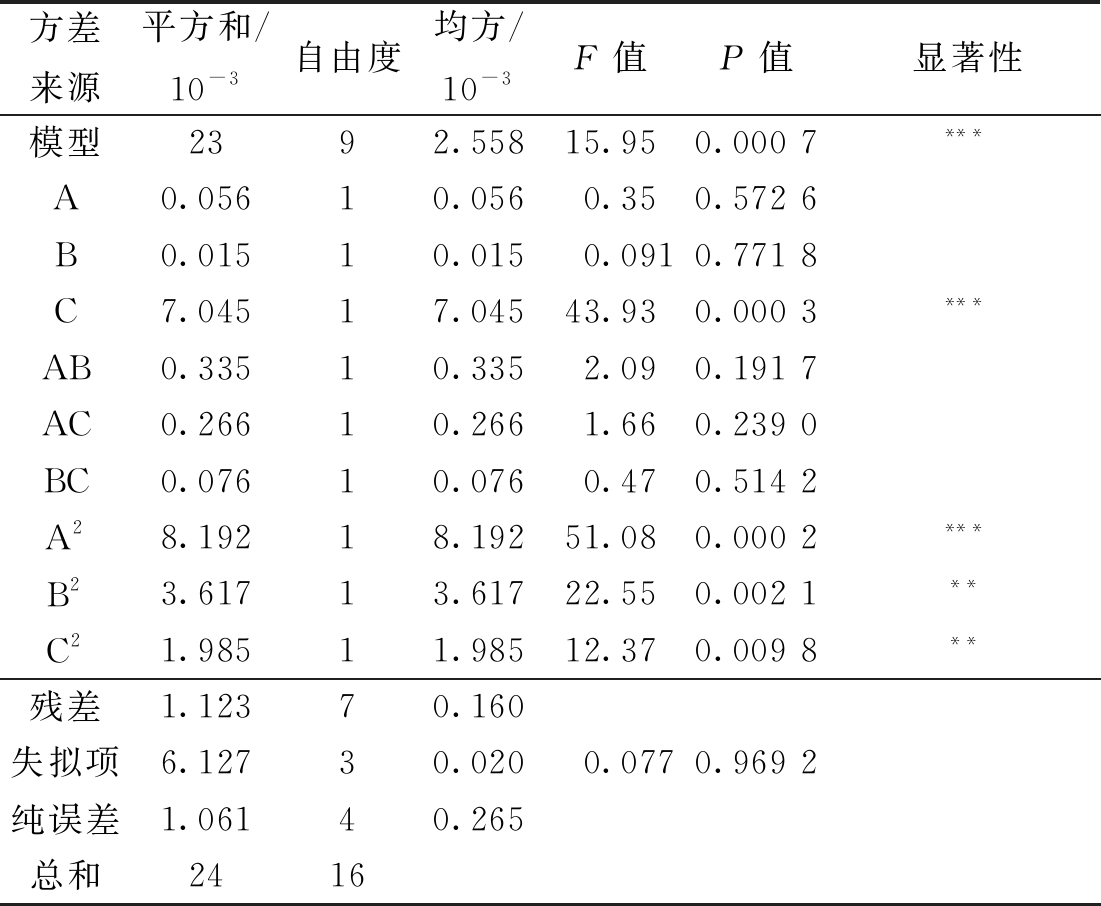
方差来源平方和/10-3自由度均方/10-3F值P值显著性模型2392.55815.950.000 7***A0.05610.0560.350.572 6B0.01510.0150.0910.771 8C7.04517.04543.930.000 3***AB0.33510.3352.090.191 7AC0.26610.2661.660.239 0BC0.07610.0760.470.514 2A28.19218.19251.080.000 2***B23.61713.61722.550.002 1**C21.98511.98512.370.009 8**残差1.12370.160失拟项6.12730.0200.0770.969 2纯误差1.06140.265总和2416
(2)各因素交互影响分析。由回归模型可得到不同因素之间交互作用的等高线和三维响应曲面图。当等高线接近椭圆时,说明两因素之间的交互作用强,影响比较明显;当等高线接近圆时,说明两因素之间的交互作用弱,相互影响不明显[11]。当一个因素不变,反应温度、pH及BBR-NH2的量三者之间的两两交互对产物BBR-DCMC的影响如图5~6所示。
由图5~6可以看出,当一个因素不变,另外两个因素对产物影响的响应面弯曲程度较大,且等高线形状呈椭圆形,说明任意两因素间的交互影响对产物生成量影响较明显。
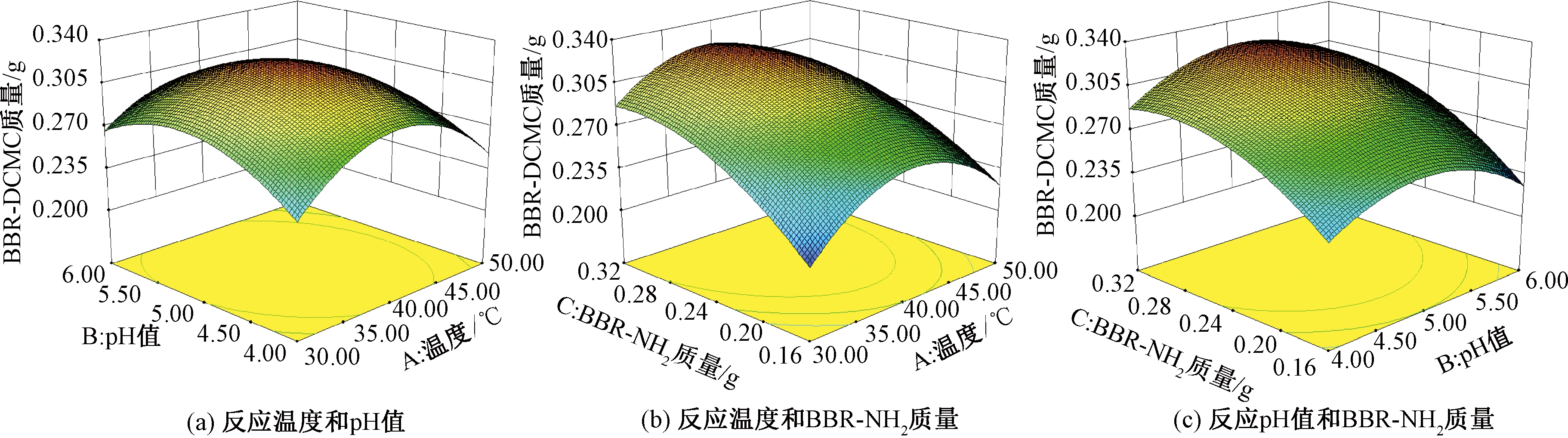
图5 反应温度和pH值对产物影响的等高线及响应面图
Figure 5 Contour and response surface diagram of the effect of reaction temperature and pH on the product
注:“*”为差异显著(P<0.05);“**”为差异高度显著(P<0.01);“***”为差异极显著(P<0.001)。
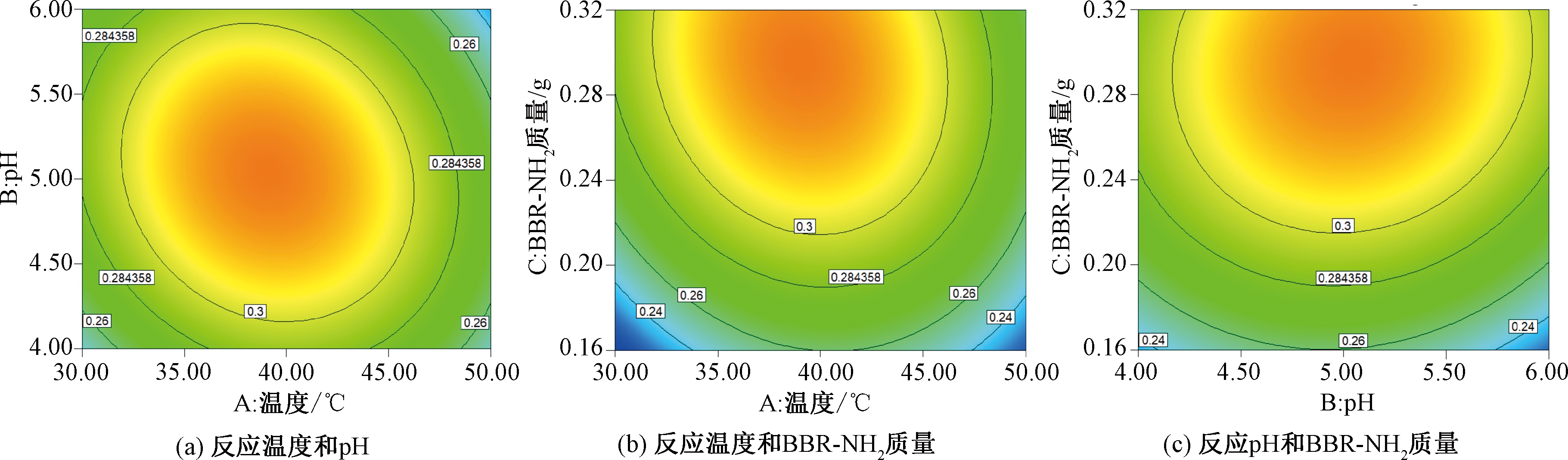
图6 反应温度和BBR-NH2质量对产物影响的等高线及响应面图
Figure 6 Contour and response surface diagram of the effect of reaction temperature and BBR-NH2 quality on the product
(3)响应面实验结果验证。当DCMC投量为0.14 g时,由响应面结果分析得最优工艺条件为BBR-NH2投量为0.30 g、反应pH值为5.05、温度为39.01 ℃,理论上产物BBR-DCMC的量为0.322 4 g。为验证响应曲面法结果的可靠性,结合实际条件,取反应温度39.0 ℃、反应pH值为5.0、BBR-NH2投料为0.30 g(双醛羧甲基纤维素与改性小檗碱质量比为7∶15),开展3次平行实验,得到BBR-DCMC的平均值为0.311 4 g,与理论值0.322 4 g接近,表明该响应面法所建立的模型真实可靠,可用于合成BBR-DCMC的工艺研究。
2.3 BBR-DCMC的表征
2.3.1 红外分析
为了研究样品结构和鉴别化合物类型,分别对CMC、DCMC、BBR-DCMC的FTIR谱图进行分析比对,如图7所示。
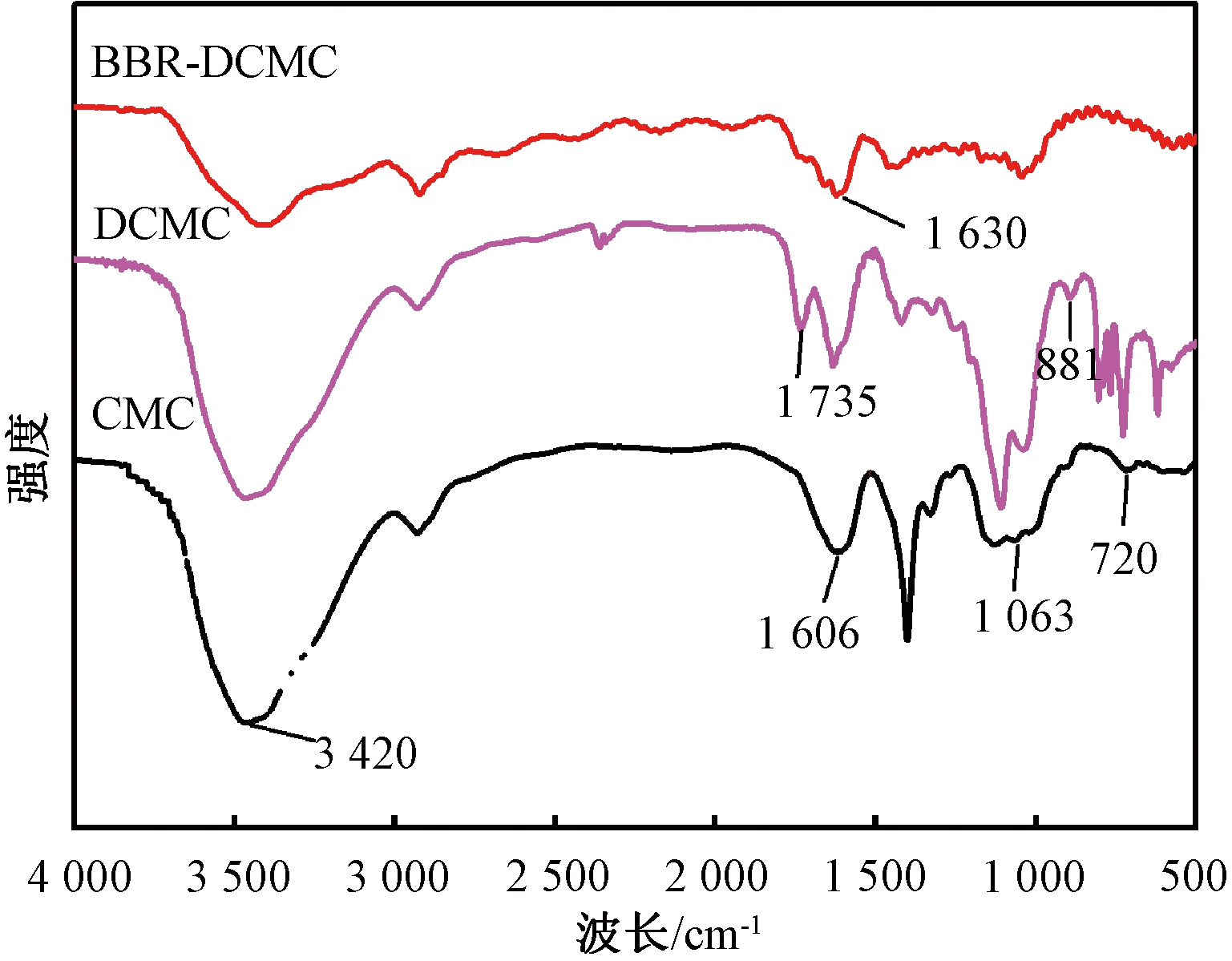
图7 CMC、DCMC和BBR-DCMC的FTIR谱图
Figure 7 FTIR spectra of CMC, DCMC and BBR-DCMC
由图7可知,CMC的FTIR谱图中,3 420 cm-1附近为O—H的伸缩振动峰;1 606 cm-1附近为基团C![]() O的伸缩振动峰;1 063 cm-1附近为CMC的C—O的伸缩振动峰;在702 cm-1附近处为O—H的面外弯曲峰[12]。DCMC的红外谱图中,3 420 cm-1附近的强峰为O—H的伸缩振动峰;当CMC被高碘酸盐氧化时,葡萄糖六元环上的C2—C3键被裂解,使每个葡萄糖单体形成两个醛基,因此在DCMC红外图谱的1 735 cm-1处出现醛基的C
O的伸缩振动峰;1 063 cm-1附近为CMC的C—O的伸缩振动峰;在702 cm-1附近处为O—H的面外弯曲峰[12]。DCMC的红外谱图中,3 420 cm-1附近的强峰为O—H的伸缩振动峰;当CMC被高碘酸盐氧化时,葡萄糖六元环上的C2—C3键被裂解,使每个葡萄糖单体形成两个醛基,因此在DCMC红外图谱的1 735 cm-1处出现醛基的C![]() O特征峰;881 cm-1附近的特征峰为醛基和邻近的羟基之间形成的半缩醛的振动吸收[10,13]。从BBR-DCMC的红外图谱可以看出,由希夫碱反应得到的纤维素基希夫碱保留了O—H、C—O和C—H的伸缩振动峰,表明产物保留了大分子的主体结构;与DCMC的峰相比,BBR-DCMC的红外图谱中C
O特征峰;881 cm-1附近的特征峰为醛基和邻近的羟基之间形成的半缩醛的振动吸收[10,13]。从BBR-DCMC的红外图谱可以看出,由希夫碱反应得到的纤维素基希夫碱保留了O—H、C—O和C—H的伸缩振动峰,表明产物保留了大分子的主体结构;与DCMC的峰相比,BBR-DCMC的红外图谱中C![]() O的缩振动峰明显减弱,说明醛基参与了反应过程;此外,产物在1 630 cm-1处出现C
O的缩振动峰明显减弱,说明醛基参与了反应过程;此外,产物在1 630 cm-1处出现C![]() N的强伸缩振动峰,这表明BBR-NH2通过席夫碱反应成功接枝到DCMC上[14]。
N的强伸缩振动峰,这表明BBR-NH2通过席夫碱反应成功接枝到DCMC上[14]。
2.3.2 XRD分析
CMC、BBR-DCMC的XRD图谱如图8所示。

图8 CMC和BBR-DCMC的XRD
Figure 8 XRD curves of CMC and BBR-DCMC
由图8可知,在2θ=20°处,CMC出现一个强衍射峰,为多糖链处于半结晶态时的特征吸峰[15];产物BBR-DCMC在2θ=20°处时也有衍射峰,且较CMC的衍射峰弱,这主要是因为高碘酸钠氧化CMC时,其原有的晶结构被破坏。其衍射峰强度降低,此过程使纤维素基分子链的内部和链间氢键被破坏,CMC内部结构变松,排列的高分子规整度变差,使高分子的结晶性能降低,也进一步证明了反应的发生。
2.3.3 TG分析
BBR-DCMC和CMC的热重测试结果如图9所示。
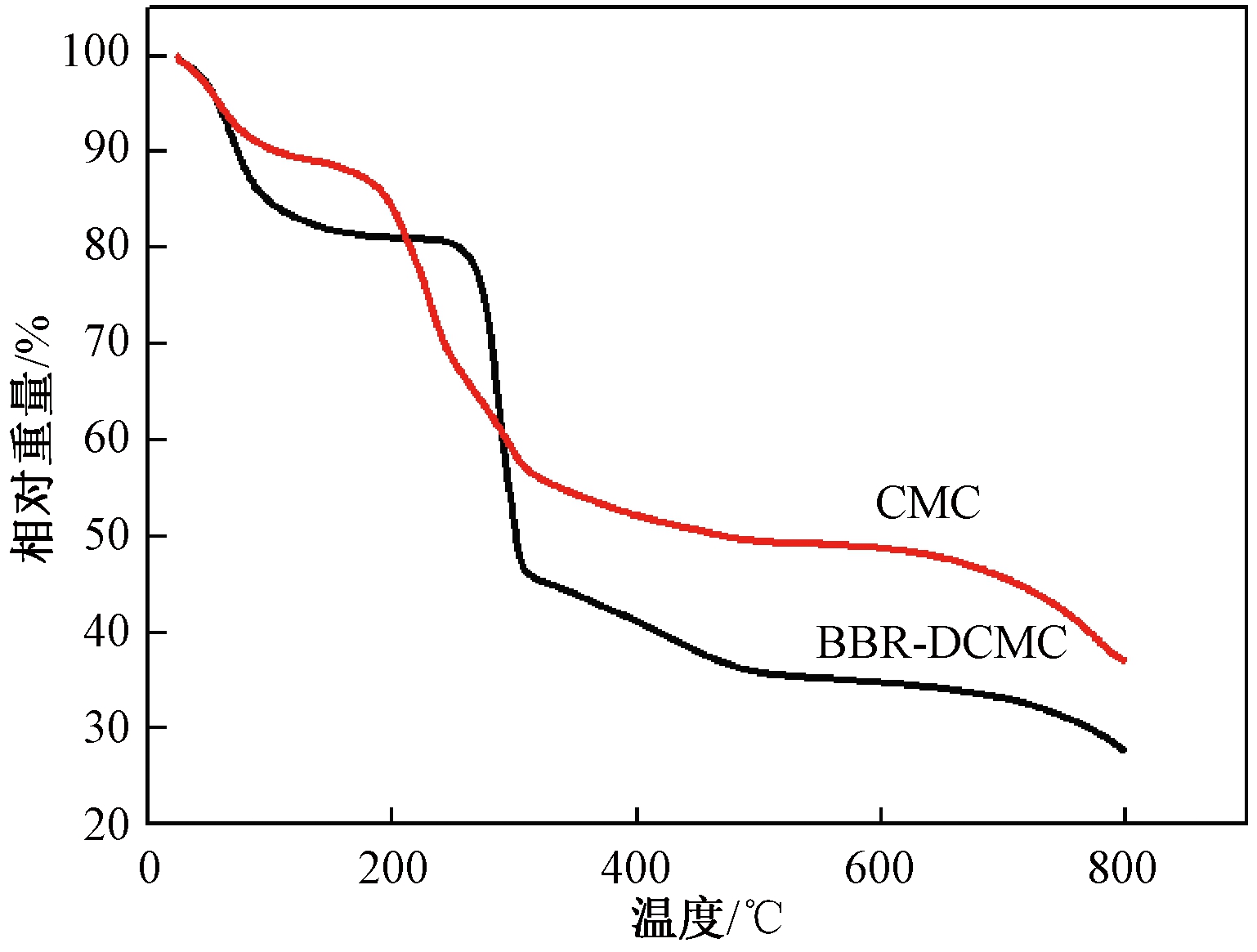
图9 CMC和BBR-DCMC的TG曲线
Figure 9 TG of CMC and BBR-DCMC
由图9可知,CMC的热裂解主要经历3个阶段。首先,当温度在23~240 ℃时,失重可达19.2%,主要是因CMC脱除物理吸附的水和结合水,可能附加去氢作用。其次,当温度为240~310 ℃时,CMC快速失重达34.6%,这可能由于CMC中的苷键、C—C键、C—H键逐渐断裂,并生成一些可挥发小分子产物。最后,当温度高于310 ℃时,CMC的剩余部分会发生芳环化,直至完全脱氢到碳化变为石墨结构[10]。将BBR接枝到DCMC上后,BBR-DCMC也表现出3个主要的质量损失阶段。第一次质量损失发生在23~160 ℃之间,可能是CMC脱水所致。160~310 ℃条件下为第二阶段质量损失,主要是高温下,CMC易分解,由于CMC的热分解所致[10]。当温度高于310 ℃时,主要是由于CMC和BBR的进一步分解、环化,直至完全碳化[13]。
2.4 抑菌防霉性能评价
采用琼脂扩散法测BBR-DCMC的抑菌效果。观察各培养基中是否出现抑菌圈,并用游标卡尺量抑菌圈大小,出现抑菌圈的最低药物浓度即为BBR-DCMC对E.coli、S.aureus、Aspergillus niger和Candiada albicans的MIC值,结果见表4。
表4 不同浓度BBR-DCMC下E.coli、S.aureus、Aspergillus niger和Candiada albicans的抑菌圈直径大小
Table 4 Diameters of inhibition zones of different concentrations of BBR-DCMC against E.coli, S.aureus,Aspergillus niger and Candiada albicans
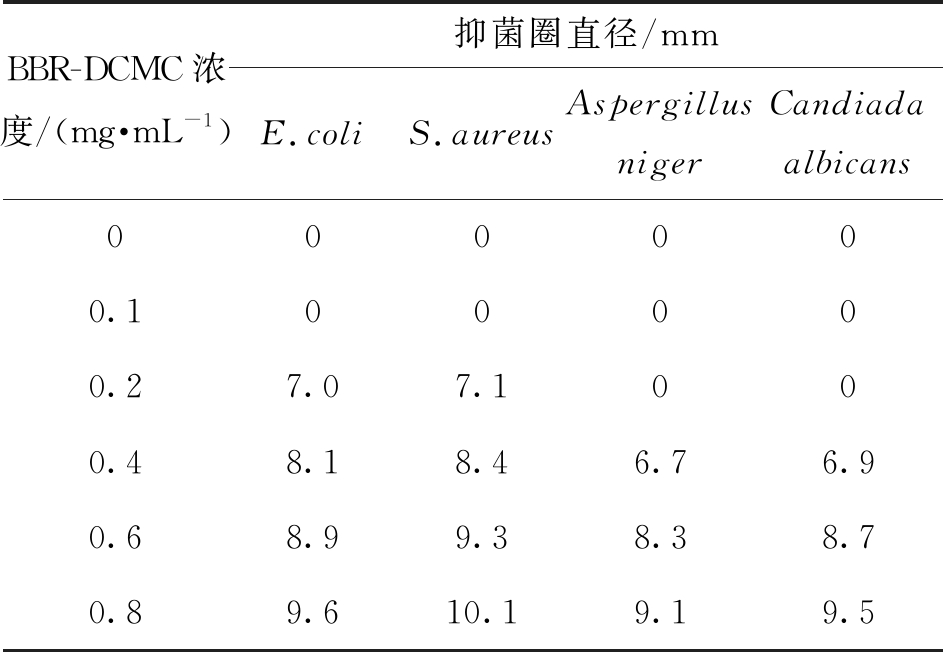
BBR-DCMC浓度/(mg·mL-1)抑菌圈直径/mmE.coliS.aureusAspergillus nigerCandiada albicans000000.100000.27.07.1000.48.18.46.76.90.68.99.38.38.70.89.610.19.19.5
由表4可知,BBR-DCMC对E.coli和S.aureus的MIC值都为0.2 mg/mL;BBR-DCMC对Aspergillus niger和Candiada albicans的MIC值都为0.4 mg/mL。随着BBR-DCMC溶液浓度升高,抑菌圈直径越大,抑菌防霉效果越强。
2.5 抑菌机理
目前,关于小檗碱的抑菌机理的研究相对较少,且作用机理尚不完全明确。BBR现有的抑菌机理研究表明主要通过菌体细胞膜通透性的改变[16],抑制相关酶和外排泵的活性[17-18],影响菌体DNA合成、mRNA转录及蛋白质的合成等[16],达到抑制菌体的效果,抑菌机理如图10所示。因抑菌机制多方位、全面化,所以细菌很难产生耐药性。
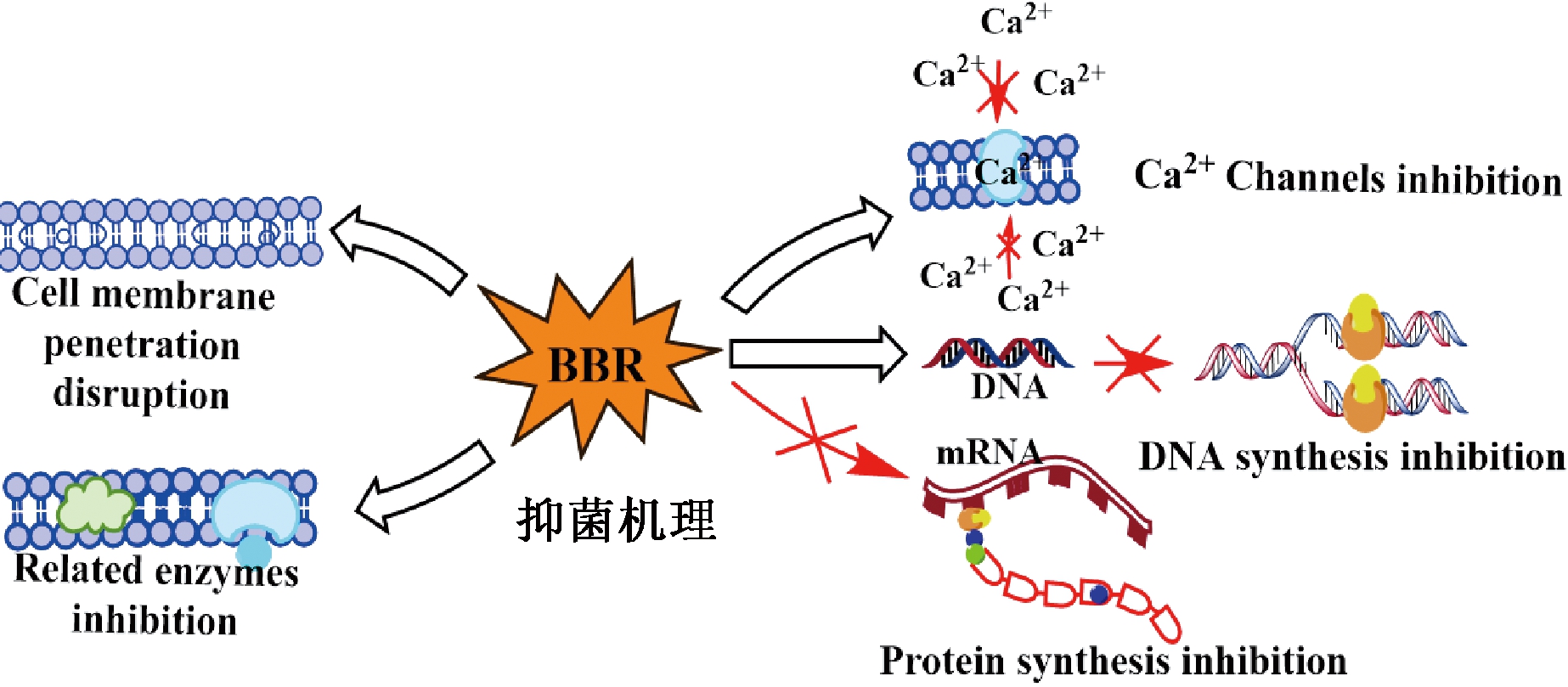
图10 BBR的抑菌机理
Figure 10 Antibacterial mechanism of BBR
3 结论
本研究以羧甲基纤维素和小檗碱为原料,通过希夫碱反应制备了BBR-DCMC,利用FTIR、XRD和TG进行表征,证明BBR-NH2被成功引入到DCMC上。通过研究反应温度、反应pH值、BBR-NH2投量对产物的影响,找到合适的工艺范围:反应温度39.0 ℃、pH值为5.0、BBR-NH2投料为0.30 g(双醛羧甲基纤维素与改性小檗碱质量比为7∶15)。由响应曲面法得到了以产物量为响应值,与反应温度、反应pH值、BBR-NH2投量因素下的二次多元回归方程Y=0.31-2.650×10-3A-1.350×10-3B+0.030C-9.150×10-3AB-8.150×10-3AC+4.350×10-3BC-0.044A2-0.029B2-0.022C2,该方程为分析合成BBR-DCMC提供了理论指导。采用琼脂纸片扩散法对BBR-DCMC进行抑菌性能的评价,证明BBR-DCMC对金黄色葡萄球菌、大肠杆菌有较好的抑菌性能。
[1] CAMARGOS C H M, FIGUEIREDO J C D, PEREIRA F V. Cellulose nanocrystal-based composite for restoration of lacunae on damaged documents and artworks on paper[J]. Journal of Cultural Heritage, 2017, 23: 170-175.
[2] HE B, LIN Q X, CHANG M M, LIU C F, et al. A new and highly efficient conservation treatment for deacidification and strengthening of aging paper by in-situ quaternization[J]. Carbohydr Polym, 2019, 209(7):250-257.
[3] LI T, WANG P L, GUO W B, et al. Natural berberine-based Chinese herb medicine assembled nanostructures with modified antibacterial application[J]. ACS Nano, 2019, 13(6): 6770-6781.
[4] POTTHAST A, AHN K. Critical evaluation of approaches toward mass deacidification of paper by dispersed particles[J]. Cellulose, 2017, 24(1): 323-332.
[5] MARTENS E, DEMAIN A L. The antibiotic resistance crisis, with a focus on the United States[J]. The Journal of Antibiotics, 2017, 70(5): 520-526.
[6] LIU Y, WANG W B, WANG A Q. Adsorption of lead ions from aqueous solution by using carboxymethyl cellulose-g-poly (acrylic acid)/attapulgite hydrogel composites[J]. Desalination, 2010, 259(1/2/3): 258-264.
[7] 孙悦. 高温纤维素降解菌的分离与鉴定研究[D]. 秦皇岛: 河北科技师范学院, 2021.
SUN Y. Study on isolation and identification of high temperature cellulose degrading bacteria[D]. Qinhuangdao: Hebei Normal University of Science & Technology, 2021.
[8] FERRANDIN-SCHOFFEL N, HAOUAS M, MARTINEAU-CORCOS C, et al. Modeling the reactivity of aged paper with aminoalkylalkoxysilanes as strengthening and deacidification agents[J]. ACS Applied Polymer Materials, 2020, 2(5): 1943-1953.
[9] 曾庆轩,张娜,邓洪斌,等.基于阻断IL-6/STAT信号通路的全新小檗碱衍生物的设计、合成及其抗炎作用评价[J].药学学报, 2017, 52(12): 1895-1902.
ZENG Q X, ZHANG N, DENG H B, et al. Design, synthesis and evaluation of anti-inflammatory effect of novel berberine derivatives on IL-6/STAT signaling pathway[J]. Acta Phaarmaccutica Sinica, 2017, 52(12): 1895-1902.
[10] LIU K, XU Y G, LIN X X, et al. Synergistic effects of guanidine-grafted CMC on enhancing antimicrobial activity and dry strength of paper[J]. Carbohydrate Polymers, 2014, 110(22): 382-387.
[11] ALDAHDOOH M A A, BUNNORI N M, JOHARI M A M. Evaluation of ultra-high-performance-fiber reinforced concrete binder content using the response surface method[J]. Engineering Failure Analysis, 2013, 52(6): 957-965.
[12] 郝超月.羧甲基纤维素钠基水凝胶的制备及其应用[D].天津:天津大学,2018.
HAO C Y. Preparation and application of sodium carboxymethylcellulose based hydrogel[D]. Tianjin: Tianjin University, 2018.
[13] 李伟雪. 羧甲基纤维素接枝偶氮色素的制备及抗还原能力的研究[D]. 天津:天津大学.
LI W X. Research on the carboxymethyl cellulose grafted azo pigment: preparation and anti-reduction property[D]. Tianjin: Tianjin University, 2017.
[14] 徐永建, 雷凤, 李伟. 纤维素基希夫碱铜配合物的制备及抗菌性能研究[J]. 2019, 38(2): 16-22.
XU Y J, LEI F, LI W. Preparation of cellulose-based schiff base-Cu complex and its antibacterial properties[J]. China Pulp & Paper, 2019, 38(2): 16-22.
[15] 吕高磊.改性羧甲基纤维素钠聚合物的合成及在水泥基材料中的应用[D].哈尔滨:东北林业大学,2018.
LYU G L. Synthesis of modified sodium carboxymethylcellulose polymers and its application in cement-based materials[D]. Harbin: Northeast Forestry University, 2018.
[16] PENG L C, KANG S, YIN Z Q, et al. Antibacterial activity and mechanism of berberine against Streptococcus agalactiae[J]. International Journal of Clinical and Experimental Pathology, 2015, 8(5): 5217-5223.
[17] KIM S H, SHIN D S, OH M N, et al. Inhibition of the bacterial surface protein anchoring transpeptidase sortase by isoquinoline alkaloids[J]. Bioscience, Biotechnology, and Biochemistry, 2004, 68(2): 421-424.
[18] WU L T, TSOU M F, HO C C, et al. Berberine inhibits arylamine N-acetyltransferase activity and gene expression in Salmonella typhi[J]. Current Microbiology, 2005, 51(4): 255-261.