0 引言
多孔碳材料由于具有超高的比表面积、优异的热稳定性和化学稳定性、可调的孔结构和孔隙率等优势,在气体吸附和分离、光电催化、能量存储和转化等领域具有广阔的应用前景[1-3]。其中多孔碳材料的化学组成可调和孔结构可控的特点促使其成为CO2捕集和电化学储能等领域最有应用前景的材料之一[4]。
根据合成方法的不同,多孔碳材料的制备可以分为水热法、活化法、模板法等[5-6]。模板法作为合成结构有序碳材料最常用的方法之一,通过采用不同模板调控多孔碳的孔结构,进而得到结构合适、孔径均一的碳材料。然而,模板法的步骤繁琐、耗时长、成本较高,从而限制了其广泛应用[7]。因此,开发廉价简便的无模板法具有重要意义。通过微孔有机聚合物碳化得到多孔碳材料的方法,由于微孔聚合物合成方法简单、单体结构选择多样、孔结构可调等优点得到了迅速的发展和广泛的关注[8],为多孔碳材料的设计提供了新的方法和思路。
孔结构和孔表面化学共同决定多孔碳材料的性能。杂原子掺杂可以调控碳骨架与客体分子之间的相互作用力[9]。微孔聚合物的单体含有各种杂原子,可以通过控制单体的比例等因素实现杂原子的可控和高效掺杂。N元素是多孔碳材料最常见也是最有效的掺杂方式,由于N原子的电负性较大,从而可以有效改变孔道微环境,提高材料极性,增加催化活性位点,提高电子传输速率[10]。双杂原子共掺杂可以进一步调控多孔碳材料的化学组成和孔结构,且N、S共掺杂的碳材料因其N和S杂原子之间的协同效应而具有更加优异的性能[11-12]。
本文通过傅克烷基化反应,以噻吩和三聚氯氰为反应单体,无水三氯化铝为催化剂,一步合成含N和S的微孔有机聚合物(PCT),进一步将PCT碳化制备N、S共掺杂微孔碳材料。重点研究了不同碳化温度对微孔碳材料在CO2捕集和超电领域应用性能的影响。
1 实验
1.1 试剂与仪器
三聚氯氰(AR,Aladdin),噻吩(AR,Aladdin),无水三氯化铝(AR,Aladdin),二氯乙烷(AR,国药),KOH(AR,国药)。
采用Thermo Nicolet iS50 FT-IR红外光谱仪和Thermo Flash EA 1112元素分析仪表征样品的化学结构,采用NETZSCH STA 449 F3同步热分析仪对样品的热稳定性进行分析,采用Hitachi S4800扫描电子显微镜观察样品的微观形貌,使用CS310电化学工作站对样品进行电化学性能表征,采用Micromeritics ASAP 2420-4MP自动表面积和孔径分析仪表征样品的孔结构和CO2吸附性能。
1.2 微孔聚合物前体PCT的制备
在N2气氛下,将三聚氯氰(1.48 g, 8 mmol)加入60 mL 1,2-二氯乙烷中,搅拌均匀后在冰浴中冷却至0 ℃,加入噻吩(0.92 mL, 12 mmol)和无水AlCl3(3.2 g, 24 mmol),搅拌反应3 h,然后升温至78 ℃,保持48 h。反应结束后,自然冷却至室温,粗产物经过滤后依次使用甲醇、丙酮和乙醇洗涤3次。再将得到的固体产物放入300 mL 6 mol/L的HCl溶液中搅拌8 h,用蒸馏水水洗至中性,随后用甲醇抽提24 h。80 ℃下真空干燥18 h得到最终产物,标记为PCT。
1.3 氮硫共掺杂微孔碳CPCT的制备
将PCT和KOH以1∶4的质量比研磨均匀,然后分散于95%乙醇中,超声4 h。旋蒸去除溶剂后,固体80 ℃真空干燥18 h,在N2气氛下碳化2 h,升温速率为2 ℃/min,然后冷却至室温。用2 mol/L HCl溶液洗涤去除过量KOH,然后用蒸馏水洗涤直至中性,80 ℃下真空干燥12 h后得到最终产物,标记为CPCT-X,其中X(5、6、7)代表碳化温度(500、600、700 ℃)。
1.4 电极制备及测试
将0.2 g微孔碳材料CPCT-X与乙炔黑在研钵中研磨30 min,使其混合均匀,滴加聚四氟乙烯乳液(三者质量比为8∶1∶1),然后滴加少量乙醇并混合均匀,呈浆状,倒于锡箔片上,制成片状,于烘箱中120 ℃烘干。将片状材料从锡箔片上揭下,剪成1 cm×1 cm的小块,称重后置于清洁的泡沫镍前端,将其翻折后使活性材料在两层泡沫镍之间,使用压片机压成电极,然后对CPCT-X电极的电化学性能进行测试。
2 结果与讨论
2.1 材料结构和形貌表征
以噻吩和三聚氯氰为反应单体,无水AlCl3为催化剂,通过简单的傅克烷基化反应一步合成含N和S杂原子的微孔聚合物PCT(图1)。
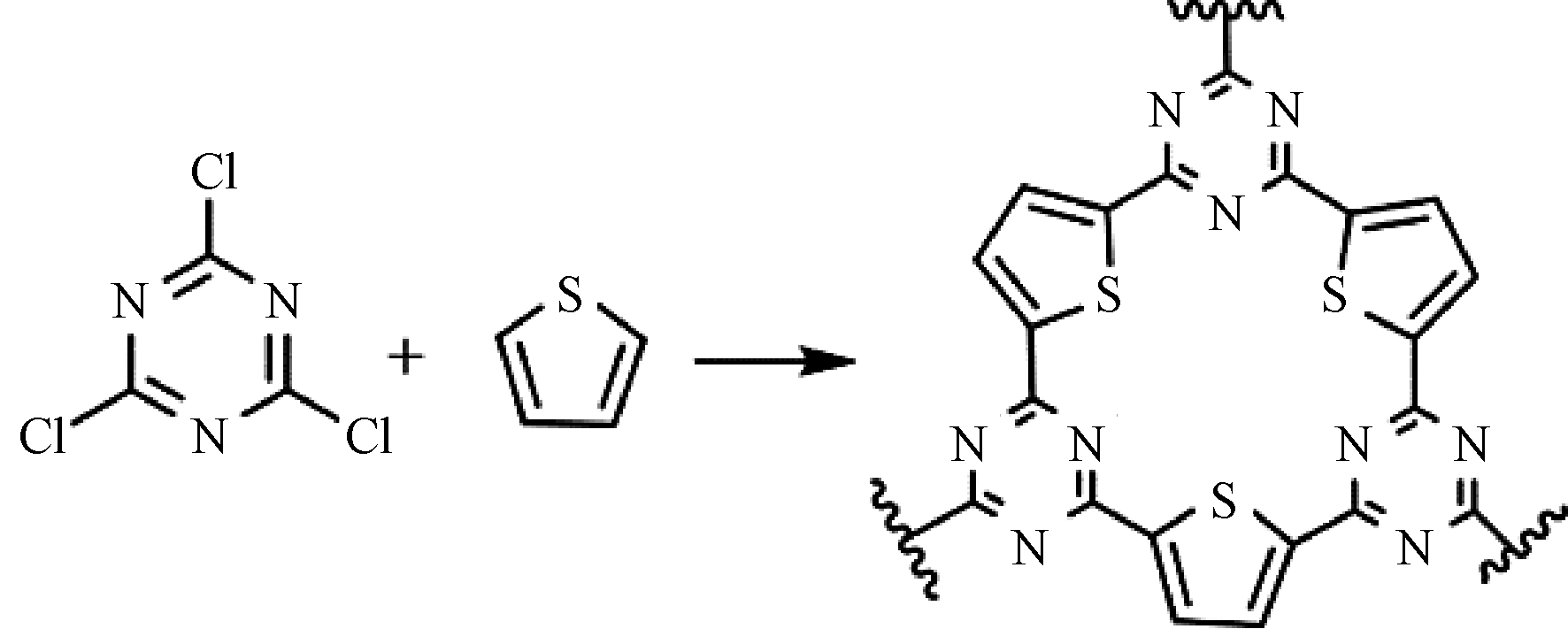
图1 PCT结构示意图
Figure 1 The structure of the PCT
从PCT的红外谱图(图2(a))中可以明显观察到C![]() N(1 626 cm-1和1 575 cm-1)和C—N(1 396 cm-1)的特征吸收峰,说明三嗪环在聚合物结构中得到保持[13]。同时,噻吩环上C─S─C的不对称伸缩振动吸收峰(1 167 cm-1和1 081 cm-1)也说明了噻吩环被成功引入所制得微孔聚合物网络中。PCT在Ar气氛中260 ℃以下几乎没有失重(图2(b)),说明微孔聚合物材料的热稳定性优异。在700 ℃时,聚合物的残余率依然达到56%,说明所得聚合物具有很高的得碳率,可以作为碳材料的前驱体。
N(1 626 cm-1和1 575 cm-1)和C—N(1 396 cm-1)的特征吸收峰,说明三嗪环在聚合物结构中得到保持[13]。同时,噻吩环上C─S─C的不对称伸缩振动吸收峰(1 167 cm-1和1 081 cm-1)也说明了噻吩环被成功引入所制得微孔聚合物网络中。PCT在Ar气氛中260 ℃以下几乎没有失重(图2(b)),说明微孔聚合物材料的热稳定性优异。在700 ℃时,聚合物的残余率依然达到56%,说明所得聚合物具有很高的得碳率,可以作为碳材料的前驱体。
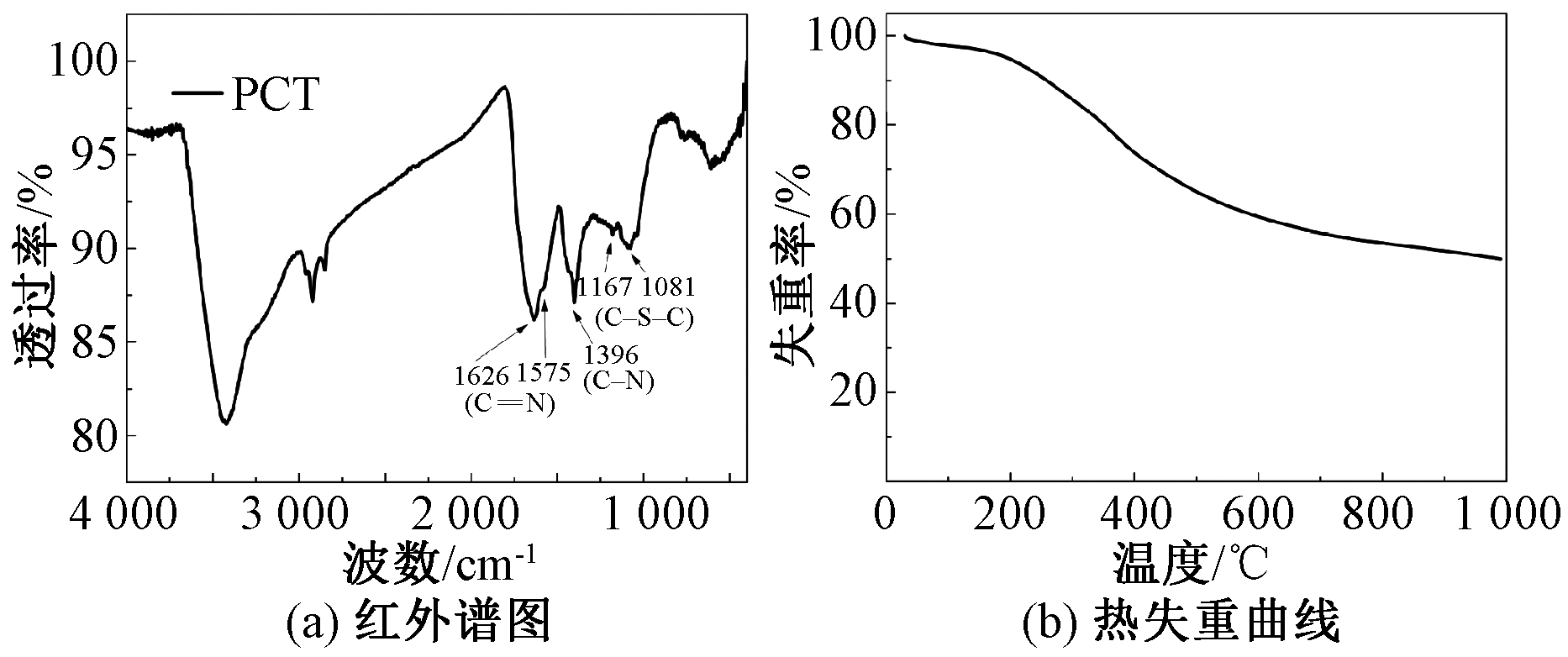
图2 碳前驱体PCT的红外谱图和热失重曲线
Figure 2 FTIR spectrum and TGA curve of PCT
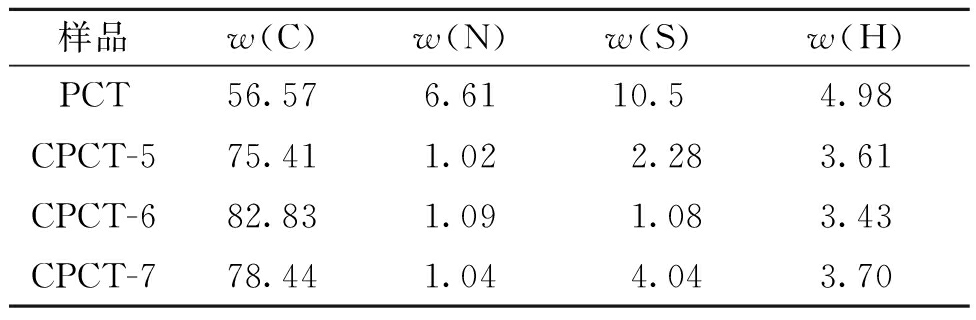
在不同温度条件下,采用氢氧化钾活化法碳化制备得到一系列N、S共掺杂微孔碳材料(CPCT-5、CPCT-6和CPCT-7)。从元素分析结果(表1)可以看出,聚合物和碳材料均含有N和S杂原子,而碳化后杂原子的含量明显减少,说明成功得到N、S共掺杂的微孔碳材料。从扫描电镜照片(图3)可以看到,N、S共掺杂微孔碳材料(CPCT-7)呈无规状,表面布满丰富的孔洞结构。
表1 PCT和CPCT-X的元素质量分数分析
Table 1 Element analysis of PCT and CPCT-X %
样品w(C)w(N)w(S)w(H)PCT56.576.6110.54.98CPCT-575.411.022.283.61CPCT-682.831.091.083.43CPCT-778.441.044.043.70

图3 CPCT-7的SEM图像
Figure 3 SEM images for the CPCT-7
2.2 N、S共掺杂微孔碳孔结构表征
从PCT的N2吸附-脱附等温线(图4)可以看出,在低相对压力下,PCT的N2吸附量上升明显,表明PCT含有微孔结构。在中压范围内,脱附曲线在吸附曲线之上,说明PCT含有介孔。在高相对压力下,PCT的氮气吸附量进一步升高,证明样品中有介孔或大孔的存在[14]。PCT的比表面积相对较低,仅为64 m2/g。
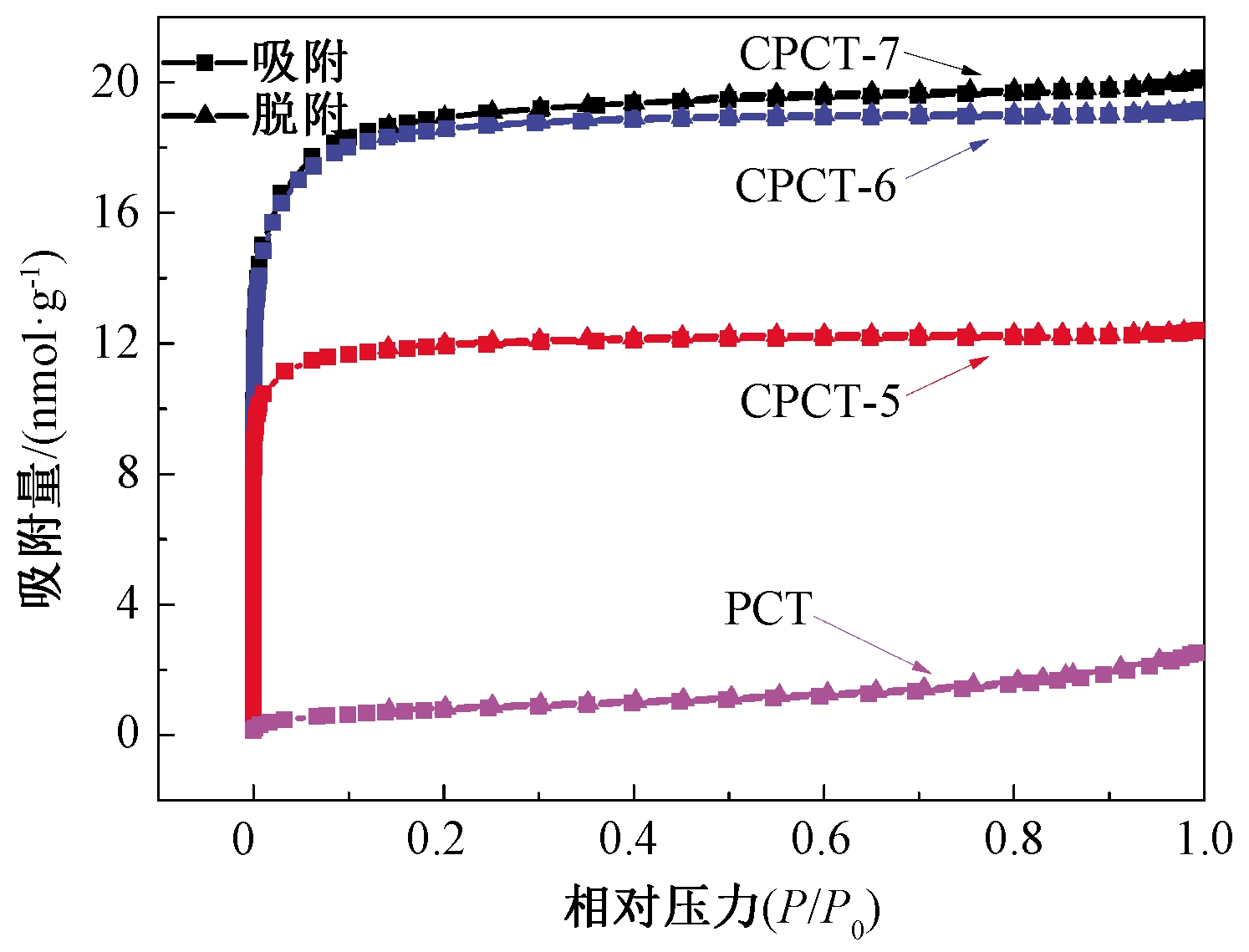
图4 PCT和CPCT-X的氮气吸附-脱附等温线
Figure 4 N2 adsorption-desorption isotherms for PCT and CPCT-X
表2 CPCT-X的孔性质
Table 2 Textural properties of CPCT-X
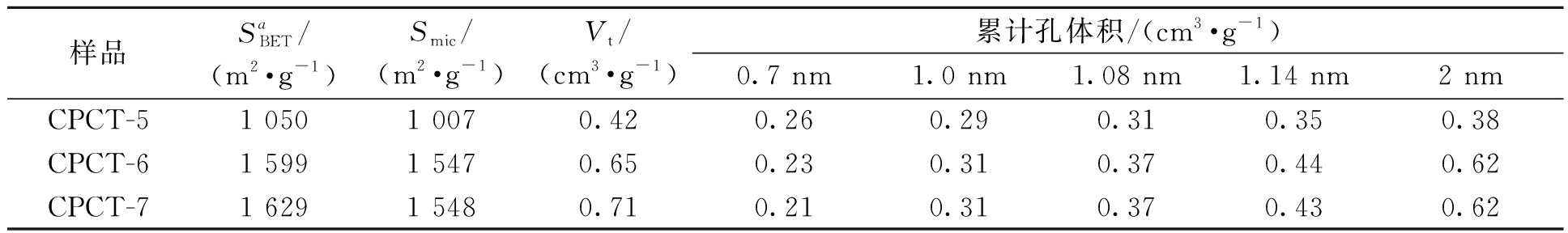
样品SaBET/(m2·g-1)Smic/(m2·g-1)Vt/(cm3·g-1)累计孔体积/(cm3·g-1)0.7 nm1.0 nm1.08 nm1.14 nm2 nmCPCT-51 0501 0070.420.260.290.310.350.38CPCT-61 5991 5470.650.230.310.370.440.62CPCT-71 6291 5480.710.210.310.370.430.62
注:![]() 为采用BET方法且使用N2吸附等温线进行计算的微孔比表面积;Smic为使用t-plot法计算的微孔比表面积;Vt为P/P0=0.99时的总孔体积。
为采用BET方法且使用N2吸附等温线进行计算的微孔比表面积;Smic为使用t-plot法计算的微孔比表面积;Vt为P/P0=0.99时的总孔体积。
PCT碳化后得到的微孔碳材料CPCT-X在低压区(图4),氮气吸附等温线呈垂直上升,吸附量远高于PCT,说明CPCT-X含有大量的微孔结构。另外CPCT-X的吸附和脱附曲线几乎重合,表明CPCT-X可以对氮气分子进行可逆吸附和脱附。
CPCT-5、CPCT-6和CPCT-7的BET比表面积随着碳化温度的升高而提高,分别为1 050 m2/g、1 599 m2/g和1 629 m2/g。当温度升高到600 ℃时,微孔碳骨架的比表面积和孔体积明显增加(表2),一方面是因为更高的温度有利于PCT的分解和热聚,另一方面高温可以促使碳酸钾进一步分解生成CO2,从而提高CPCT-X的孔隙度[15]。CPCT-6的比表面积为CPCT-5的1.53倍,而CPCT-7的比表面积与CPCT-6相差不大,考虑节能因素,600 ℃为最佳碳化温度。与此同时,CPCT-X的孔径绝大部分位于2 nm以内,微孔孔隙率分别达到95.9%、96.7%、95.0%,远高于其他文献报道的微孔碳材料[16]。高的微孔孔隙率可以为客体分子提供有效的空间,提高此类微孔碳材料的应用性能。
2.3 N、S共掺杂微孔碳材料的CO2吸附性能
CPCT-X在273 K和298 K下对CO2的吸附性能如图5和表3所示。CPCT-6对CO2具有很高的吸附量,可达5.5 mmol/g(273 K,0.1 MPa)和3.2 mmol/g(298 K,0.1 MPa),优异的CO2吸附性能与材料的杂原子掺杂和丰富的微孔具有直接关系。尤其是超微孔(<0.7 nm)对CO2的吸附性能起关键作用。在0.015 MPa下,CPCT-X在273 K和298 K的CO2吸附量均与超微孔的体积呈正比关系。
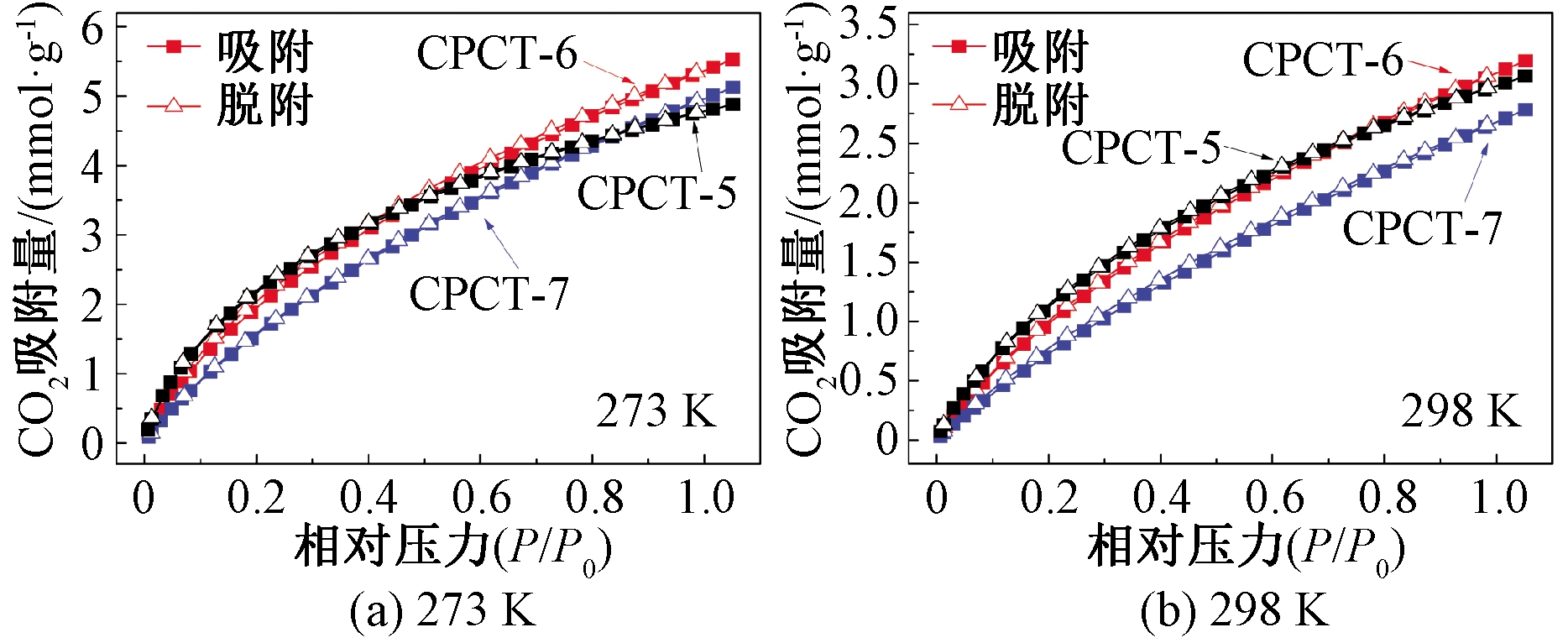
图5 CPCT-X的CO2吸附-脱附等温线
Figure 5 CO2 adsorption-desorption isotherms of CPCT-X
表3 CPCT-X的CO2吸附量
Table 3 CO2 adsorption capacities of CPCT-X
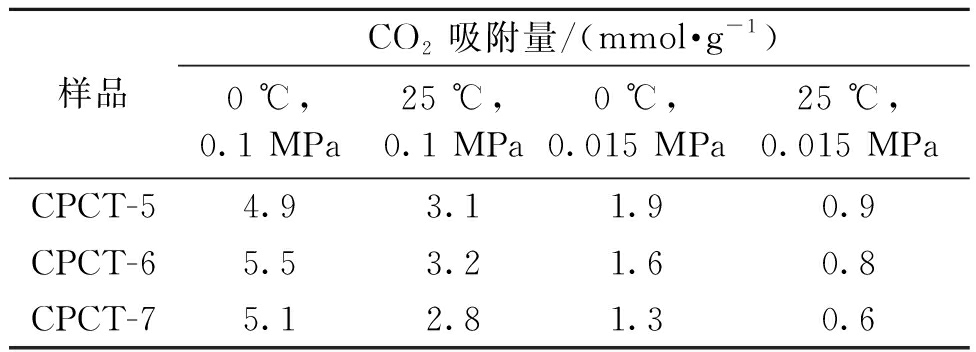
样品CO2吸附量/(mmol·g-1)0 ℃, 0.1 MPa25 ℃, 0.1 MPa0 ℃, 0.015 MPa25 ℃, 0.015 MPaCPCT-54.93.11.90.9CPCT-65.53.21.60.8CPCT-75.12.81.30.6
从CPCT-X对CO2的等量吸附热(Qst)曲线(图6)可以看出,在低CO2覆盖下,CPCT-5、CPCT-6和CPCT-7的CO2吸附热分别为33.3 kJ/mol、31.5 kJ/mol和31.0 kJ/mol,与它们的超微孔体积的大小趋势一致,说明超微孔体积可以影响材料的吸附热,改变材料与CO2之间的作用力,从而提高CO2的吸附量。
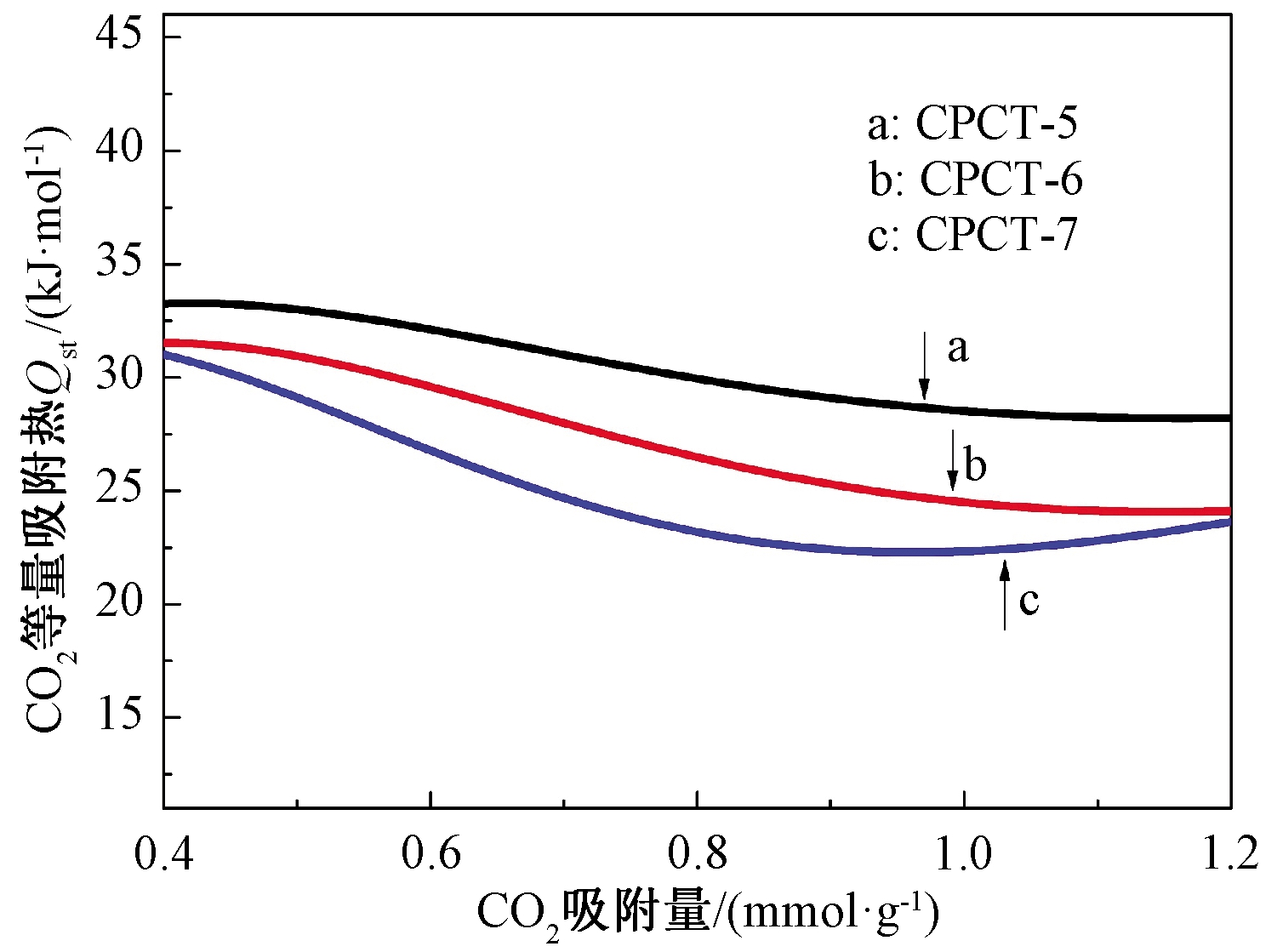
图6 CPCT-X的等量吸附热
Figure 6 The isosteric heat (Qst) of CPCT-X
2.4 N和S共掺杂微孔碳超级电容器性能
采用三电极体系对CPCT-X的电化学性能进行表征,电压为-1~0 V,电解质为6 mol/L KOH溶液。从图7中可以看出,CPCT-6有近似矩形的循环伏安曲线,证明CPCT-6具有双电层电容储能机理,即电荷在其表面为吸附和脱附过程。另外,由于N和S杂原子的掺杂,在材料中引入了部分赝电容,从而导致矩形形状的轻微扭曲。在200 mV/s的扫速下,材料的循环伏安曲线形状得到较好的保持,说明CPCT-6具有较好的倍率稳定性能。
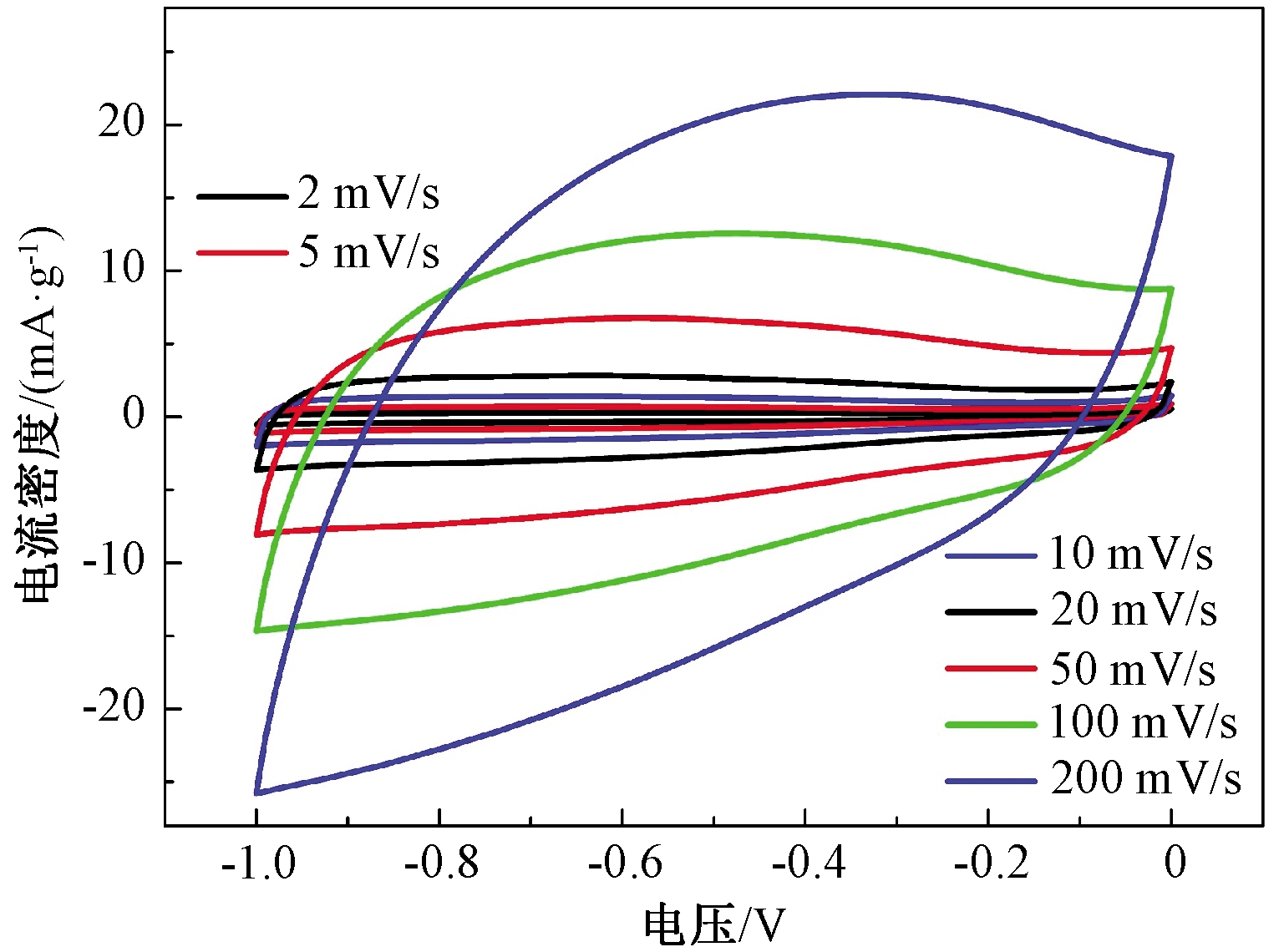
图7 不同扫速下CPCT-6的CV曲线
Figure 7 The CV curves of CPCT-6 at different scan rates
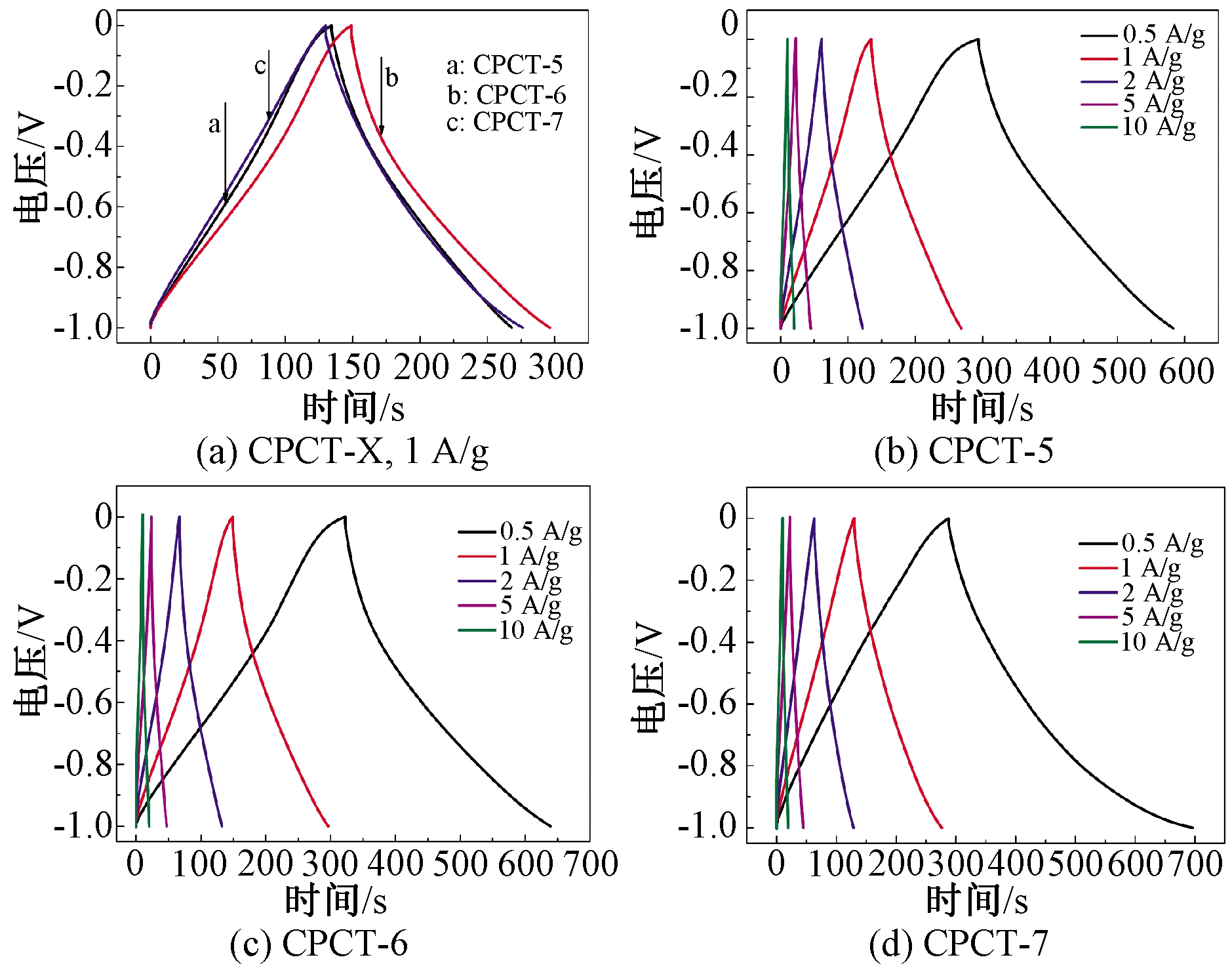
图8 CPCT-X在1 A/g电流密度下以及CPCT-5、CPCT-6和CPCT-7在不同电流密度下的恒流充放电曲线
Figure 8 Galvanostatic charge/discharge curves of the CPCT-X electrodes at a current density of 1 A/g and CPCT-5, CPCT-6, CPCT-7 at different current densities
从恒流充放电曲线图8(a)可以看出,在1 A/g电流密度下,CPCT-5、CPCT-6和CPCT-7的恒流充放电曲线呈等腰三角形的形状,并具有轻微的弧,证明了CPCT-X的储能机理中双电层电容和赝电容同时存在,其中双电层电容占主导地位,与前面的结果相吻合。同时随着电流密度的增加,CPCT-X的充放电曲线依然保持典型的三角形形状,如图8(b)~8(d)所示,说明样品具有较好的电容行为。通过计算,在电流密度为1 A/g下,CPCT-5、CPCT-6和CPCT-7的比电容(Cm)分别为137、154、152 F/g。Cm值随着充放电流密度的增大呈减小趋势,主要是因为离子在高电流密度下不易扩散,难以渗透到材料内部,充放电行为无法完全进行。相对1 A/g,当电流密度增加到10 A/g时,CPCT-5、CPCT-6和CPCT-7的Cm保持率分别达到83%、85%和75%,说明CPCT-X具有较好的倍率性能。这主要是因为碳材料中N和S共掺杂协同效应提高了材料的表面极性,从而减小了电解液离子的电阻;同时,N、S两种杂原子可以充当活性位点,在充放电过程中引入赝电容。另外,材料丰富的孔结构有利于电解质离子的快速转移和扩散。在低电流密度0.5 A/g下,CPCT-7具有高的比电容,可达210 F/g,然而其倍率性能最低,这可能与材料的S含量有关。相对于CPCT-5和CPCT-6而言,CPCT-7的硫含量最高,过高的S原子含量可能会加剧碳材料石墨化结构的扭曲和破坏,从而导致导电性降低,其倍率稳定性随之下降。从CPCT-X的交流阻抗谱图(图9)中可以看到,这3种材料在低频区的斜率很高,在高频区的半圆也不明显,说明它们的内阻较小。
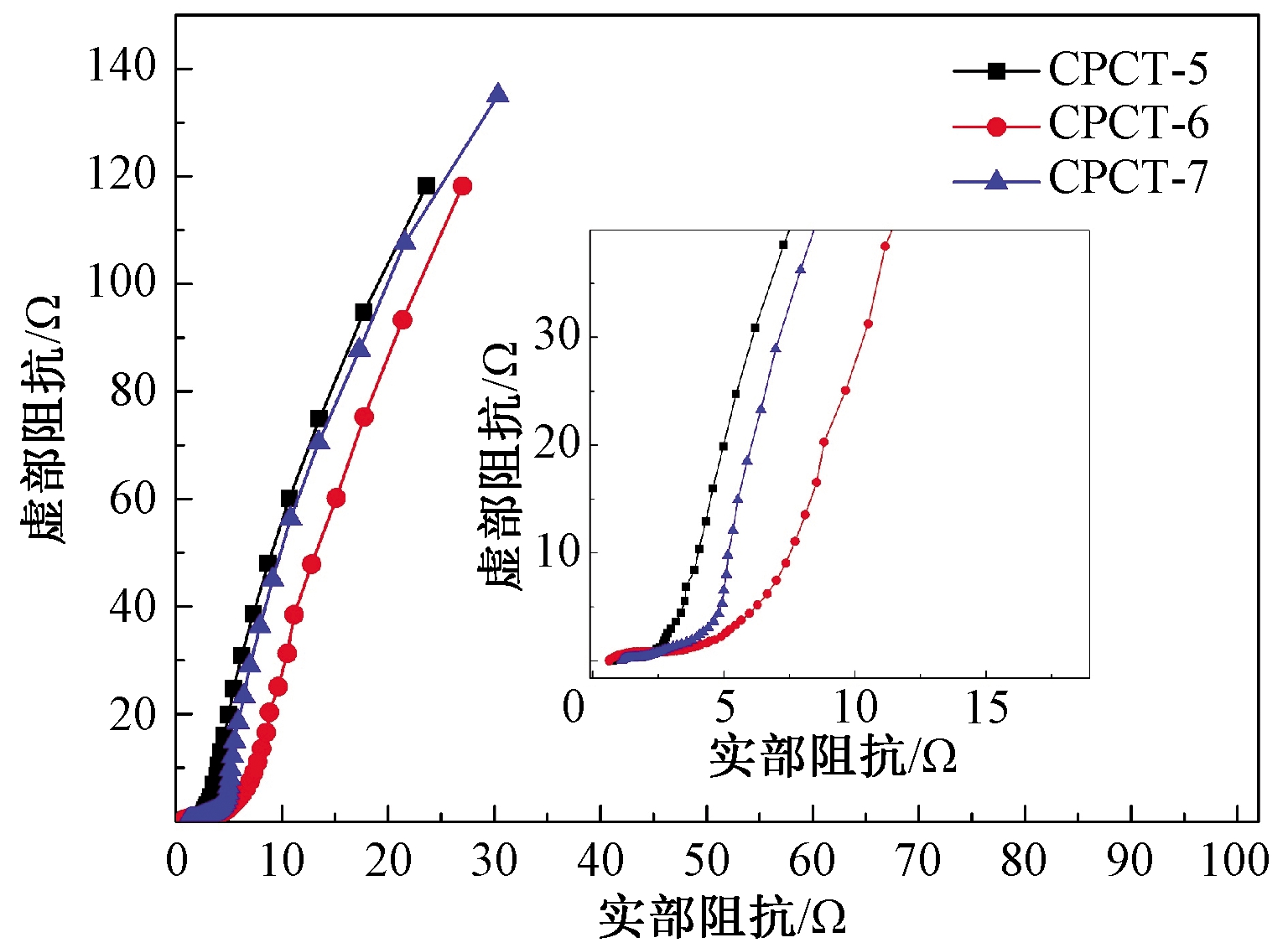
图9 CPCT-X的Nyquist曲线
Figure 9 Nyquist plots of CPCT-X
3 结论
以噻吩和三聚氯氰为单体,通过简单的傅克烷基化反应一步合成含N、S微孔聚合物,并进一步碳化得到N、S共掺杂的微孔碳材料。该碳材料具有较大的比表面积(1 050~1 629 m2/g)和超高的微孔孔隙率(95.0%~96.7%),并具有优异的CO2吸附性能,在0 ℃和25 ℃下对CO2的吸附量分别为4.9~5.5 mmol/g和2.8~3.2 mmol/g,杂原子掺杂和超微孔结构对材料的CO2吸附性能具有关键作用。同时,所得N、S共掺杂微孔碳还具有很好的超级电容器性能,当电流密度为0.5 A/g时,材料的比电容最高可达210 F/g。N和S的掺杂增强了材料的亲水性,减小了电解液离子的电阻,材料丰富的孔结构有利于电解质离子的快速转移和扩散。
[1] WICKRAMARATNE N P, JARONIEC M. Activated carbon spheres for CO2 adsorption[J]. ACS applied materials & interfaces, 2013, 5(5): 1849-1855.
[2] TIAN Z H, HUANG J J, ZHANG Z L, et al. Organic-inorganic hybrid microporous polymers based on Octaphenylcyclotetrasiloxane: synthesis, carbonization and adsorption for CO2[J]. Microporous and mesoporous materials, 2016, 234: 130-136.
[3] LIU J, WICKRAMARATNE N P, QIAO S Z, et al. Molecular-based design and emerging applications of nanoporous carbon spheres[J]. Nature materials, 2015, 14(8): 763.
[4] BING X F, WEI Y J, WANG M, et al. Template-free synthesis of nitrogen-doped hierarchical porous carbons for CO2 adsorption and supercapacitor electrodes[J]. Journal of colloid and interface science, 2017, 488: 207-217.
[5] LAKHI K S, PARK D H, AL-BAHILY K, et al. Mesoporous carbon nitrides: synthesis, functionalization, and applications[J]. Chemical society reviews, 2017, 46(1): 72-101.
[6] MA G F, YANG Q, SUN K J, et al. Nitrogen-doped porous carbon derived from biomass waste for high-performance supercapacitor[J]. Bioresource techno-logy, 2015, 197: 137-142.
[7] WU D C, DONG H C, PIETRASIK J, et al. Novel nanoporous carbons from well-defined poly (styrene-co-acrylonitrile)-grafted silica nanoparticles[J]. Chemistry of materials, 2011, 23(8): 2024-2026.
[8] TAN L X, TAN B E. Hypercrosslinked porous polymer materials: design, synthesis, and applications[J]. Chemical society reviews, 2017, 46(11): 3322-3356.
[9] UPPUGALLA S, MALE U, SRINIVASAN P. Design and synthesis of heteroatoms doped carbon/polyaniline hybrid material for high performance electrode in supercapacitor application[J]. Electrochimica acta, 2014, 146: 242-248.
[10] LI W Z, LI B Y, SHEN M, et al. Use of Gemini surfactant as emulsion interface microreactor for the synthesis of nitrogen-doped hollow carbon spheres for high-performance supercapacitors[J]. Chemical engineering journal, 2020, 384:123309.
[11] BAIRI V G, NASINI U B, RAMASAHAYAM S K, et al. Electrocatalytic and supercapacitor performance of phosphorous and nitrogen co-doped porous carbons synthesized from aminated tannins[J]. Electrochimica acta, 2015, 182: 987-994.
[12] JIA Q, YANG C, PAN Q Q, et al. High-voltage aqueous asymmetric pseudocapacitors based on methyl blue-doped polyaniline hydrogels and the derived N/S-codoped carbon aerogels[J]. Chemical engineering journal, 2020, 383: 123153.
[13] TROSCHKE E, GR TZ S, LÜBKEN T, et al. Mechanochemical Friedel-Crafts alkylation—A sustainable pathway towards porous organic polymers[J]. Angewandte chemie, 2017, 129(24): 6963-6967.
TZ S, LÜBKEN T, et al. Mechanochemical Friedel-Crafts alkylation—A sustainable pathway towards porous organic polymers[J]. Angewandte chemie, 2017, 129(24): 6963-6967.
[14] TIAN Z H, HEIL T, SCHMIDT J, et al. Synthesis of a porous C3N-derived framework with high yield by gallic acid cross-linking using salt melts[J]. ACS applied materials & interfaces, 2020, 12(11): 13127-13133.
[15] SRINIVAS G, BURRESS J, YILDIRIM T. Graphene oxide derived carbons (GODCs): synthesis and gas adsorption properties[J]. Energy & environmental science, 2012, 5(4): 6453-6459.
[16] LI Z H, WU D C, LIANG Y R, et al. Facile fabrication of novel highly microporous carbons with superior size-selective adsorption and supercapacitance properties[J]. Nanoscale, 2013, 5(22): 10824-10828.