0 引言
盐酸氟桂利嗪(flunarizine hydrochloride,FH),是双氟呱嗪类衍生物,是一种选择性钙离子通道阻隔剂[1].临床应用中,大多用来防治神经系统疾病和脑血管病[2].有研究表明,若能将FH粒径缩小到微纳米级尺寸,可以降低在非靶向部位的分布,直接作用于脑部,提高药物的利用率,减小服用剂量,降低毒副作用.
传统的药物微粒化技术如机械磨碎、喷雾干燥或重结晶等易产生化学降解、溶剂残留、温度高致药物失活、微粒尺寸大且分布较宽等问题[3].超临界溶液快速膨胀法(rapid expansion of supercritical solution,RESS)克服了传统的药物微粒化技术的缺点,具有操作条件温和、制备的微粒尺寸分布均匀、粒子流动性好、结晶纯度高;无溶剂残余、洁净环保;工艺简单等优势,成为在医药领域被广泛应用的新型药物微粒化技术[4].陈琪等[5]使用RESS法制备了醋酸泼尼松微粒.Yim等[6]使用RESS法制备了阿德福韦酯超微粉体微粒.Baseri等[7]使用RESS法制备了平均粒径为2.2 μm的二甲苯氧庚酸微粒.
笔者在前期研究了FH在超临界流体(Su-percritical Fluid, SCF)中的溶解度的基础上,首次采用RESS法制备出了FH药物微粒,重点考察夹带剂用量、萃取温度、萃取压力、膨胀室温度、喷嘴温度、喷嘴直径等对微粒形貌等的影响.采用扫描电镜(scanning electron microscope, SEM)、傅里叶红外光谱(fourier transform infrared, FT-IR)、X射线衍射(X-ray diffraction,XRD)以及热重分析(thermogravimetric analysis, TGA)分别对FH原料药和药物微粒进行表征分析.
1 实验部分
1.1 实验材料与仪器
实验材料.盐酸氟桂利嗪(药用级,含量99%,武汉大华伟业医药化工有限公司,批号20160506);无水乙醇(分析纯,含量≥99.7%,天津市风船化学试剂有限公司);溴化钾(色谱纯,天津光复科技发展有限公司).
实验仪器.Helix-7409型超临界装置(美国分离有限公司);JSM-7500F型扫描电镜(日本电子公司);XSP-8cz型光学显微镜(上海兴行实业有限公司);X′Pert PRO X射线衍射仪(荷兰帕纳科公司);Thermo Scientific Nicolet iS5型红外光谱仪(赛默飞世尔科技有限公司);DTG/DSC-60型热重分析仪(日本岛津公司);AX224ZH/E型分析天平(奥豪斯仪器(常州)有限公司).
1.2 实验方法
RESS制备FH微粒的原理:由于固体溶质FH在SCF中的溶解度随SCF的密度变化而发生变化,把需要微粒化的FH溶解到SCF中,再将溶有FH的超临界溶液经喷嘴,在极短时间内快速膨胀到低压低温的膨胀室,膨胀过程中会形成机械扰动,该扰动是以音速进行传递的,膨胀后的气体迅速达到高度的过饱和状态,从而使得溶解在其中的FH 瞬间生成大量的晶核,同时在均匀的环境中短时间内迅速长大,最终得到大量平均粒径小且分布均匀的FH微粒的过程[8].
1.3 实验内容
1.3.1 FH微粒化过程的单因素实验
(1)夹带剂用量.选择夹带剂的流速为0.2~0.6 mL/min.其他条件为:萃取温度45 ℃,萃取压力10 MPa,膨胀室温度100 ℃,喷嘴温度150 ℃,喷嘴直径为50 μm.
(2)萃取温度.选择萃取温度为35~55 ℃.其中夹带剂流速为0.2 mL/min,其他条件同(1).
(3)萃取压力.选择萃取压力为10~30 MPa.其中夹带剂流速为0.2 mL/min,其他条件同(1).
(4)膨胀室温度.分别选择膨胀室温度为100、110、120、130、140 ℃,其他条件同(1).
(5)喷嘴温度.在RESS中,由于超临界流体溶液经喷嘴膨胀的过程中要吸收大量的热,为了防止超临界流体在喷嘴处冷凝,堵塞喷嘴,在喷射过程中需要不断地对喷嘴进行加热,分别选择喷嘴温度为110、120、130、140、150 ℃,其他条件同(1).
(6)喷嘴直径.在采用RESS法制备固体物质微粒的实验中,颗粒的大小和形貌受喷嘴结构、喷射距离、直径的影响.本实验的装置中,结构和距离都是固定的,所以只研究喷嘴直径的影响.所选用的喷嘴直径为50、75、100 μm,其他条件同(1).
1.3.2 FH微粒化过程的正交实验设计
采用正交实验方法完成实验方案的工艺优化,选择萃取温度(T1/℃)、萃取压力(P/MPa)、喷嘴温度(T2/℃)、夹带剂用量(Q/mL·min-1)4个影响因素,根据正交实验表选取L9(34)正交表,正交设计见表1.
表1 正交实验设计表及结果分析
Tab.1 Orthogonal experiment design and results analysis
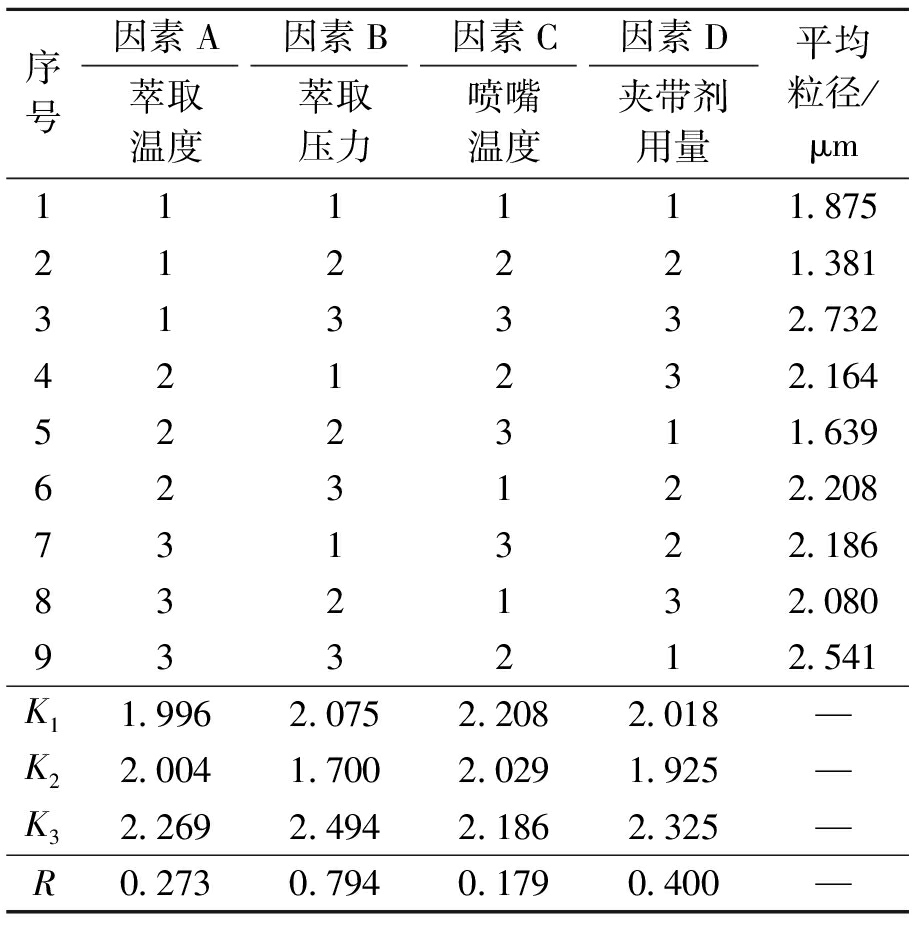
序号因素A因素B因素C因素D萃取温度萃取压力喷嘴温度夹带剂用量平均粒径/μm111111.875212221.381313332.732421232.164522311.639623122.208731322.186832132.080933212.541K11.9962.0752.2082.018—K22.0041.7002.0291.925—K32.2692.4942.1862.325—R0.2730.7940.1790.400—
2 结果与讨论
2.1 RESS制备FH微粒的单因素结果
不同夹带剂用量、萃取温度、萃取压力、膨胀室温度、喷嘴温度和喷嘴直径下的微粒平均粒径如图1所示.微粒的粒径分布如图2所示.
(1)夹带剂用量的影响.由图1(a)、图2(a)可知,随着夹带剂流速的提高,FH微粒的平均粒径增加,流速从0.2 mL/min提高到0.6 mL/min,FH微粒的平均粒径从1.959 μm增加到了6.893 μm.随着夹带剂用量的增大,无水乙醇在SCF中的浓度增加,则FH的溶解度提高,夹带剂在膨胀过程中因温度降低会导致FH析出,容易出现晶体的二次结晶现象,因此使制备的微粒粒径增大.实验结果表明,RESS中夹带剂的用量在0.2 mL/min左右时更有利于得到粒径小、尺寸分布均匀的FH药物微粒.
(2)萃取温度的影响.由图1(b)、图2(b)可知,随着萃取温度的升高,FH微粒的平均粒径增加.萃取温度从35 ℃升高到55 ℃,FH的平均粒径从1.795 μm增加到2.998 μm.这是由于随着萃取温度的升高,FH 在SCF中的浓度增大,在膨胀过程中发生团聚,导致粒度增加.故在较低的萃取温度下,更有利于制备粒径小且分布均匀的FH药物微粒.
(3)萃取压力的影响.由图1(c)、图2(c)可知,RESS法得到的FH微粒粒径随着压力的升高而降低.这是由于压力增大,FH 在SCF中的溶解度也增大,在喷嘴处的过饱和度增加,喷射时成核速率增加,形成的微核的临界半径减小;同时,随着萃取压力的升高,从喷嘴出来的超临界流体的扰动增强,流速增大,微粒的停留时间减小,聚集几率降低,得到的微粒粒径度小.
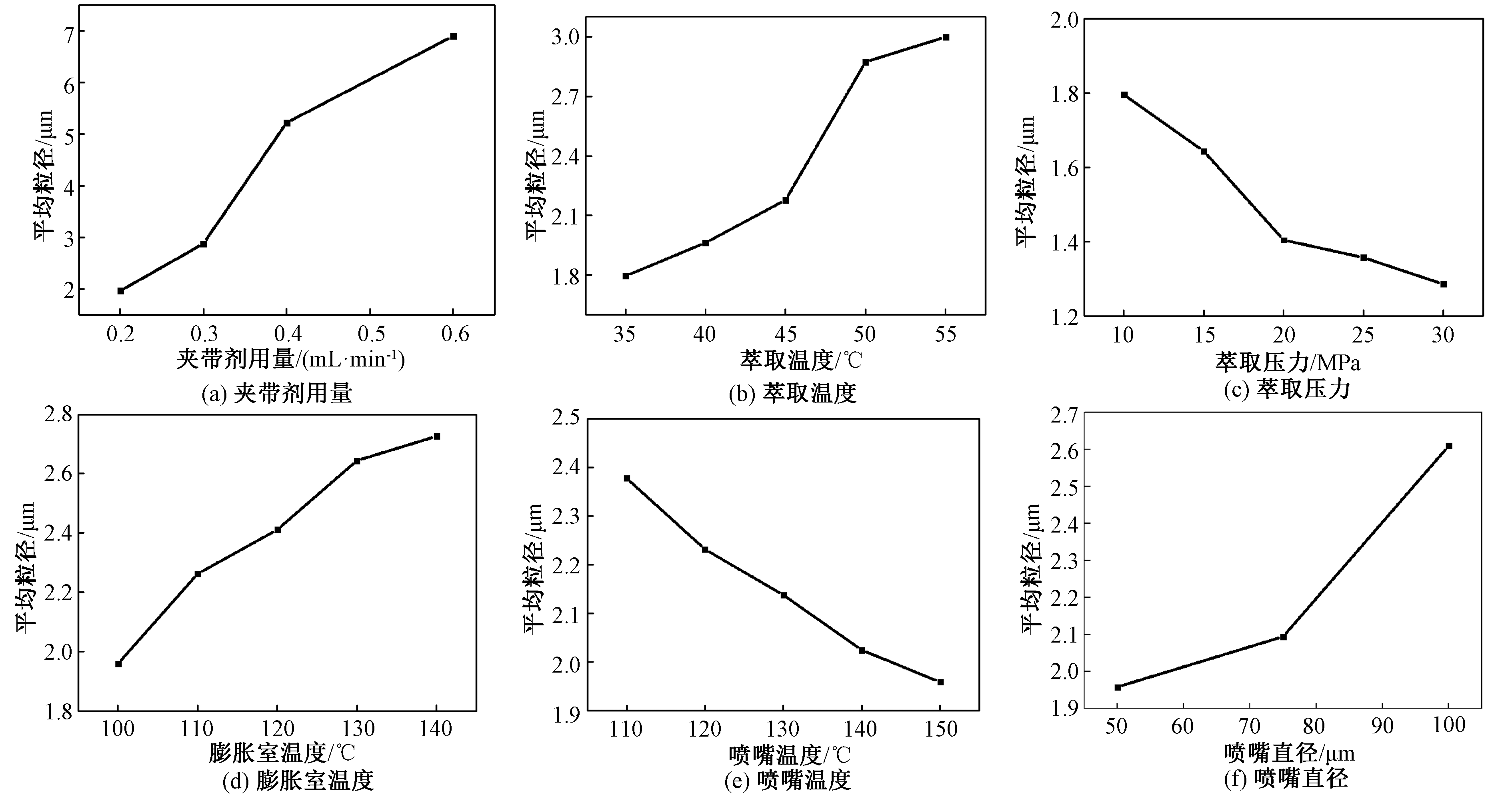
图1 不同的夹带剂用量、萃取温度、萃取压力、膨胀室温度、喷嘴温度和喷嘴直径的微粒平均粒径
Fig.1 The average particle size under different of entrainer dosage, extraction temperature, extraction pressure, expansion chamber temperatures, nozzle temperature and nozzle diameter
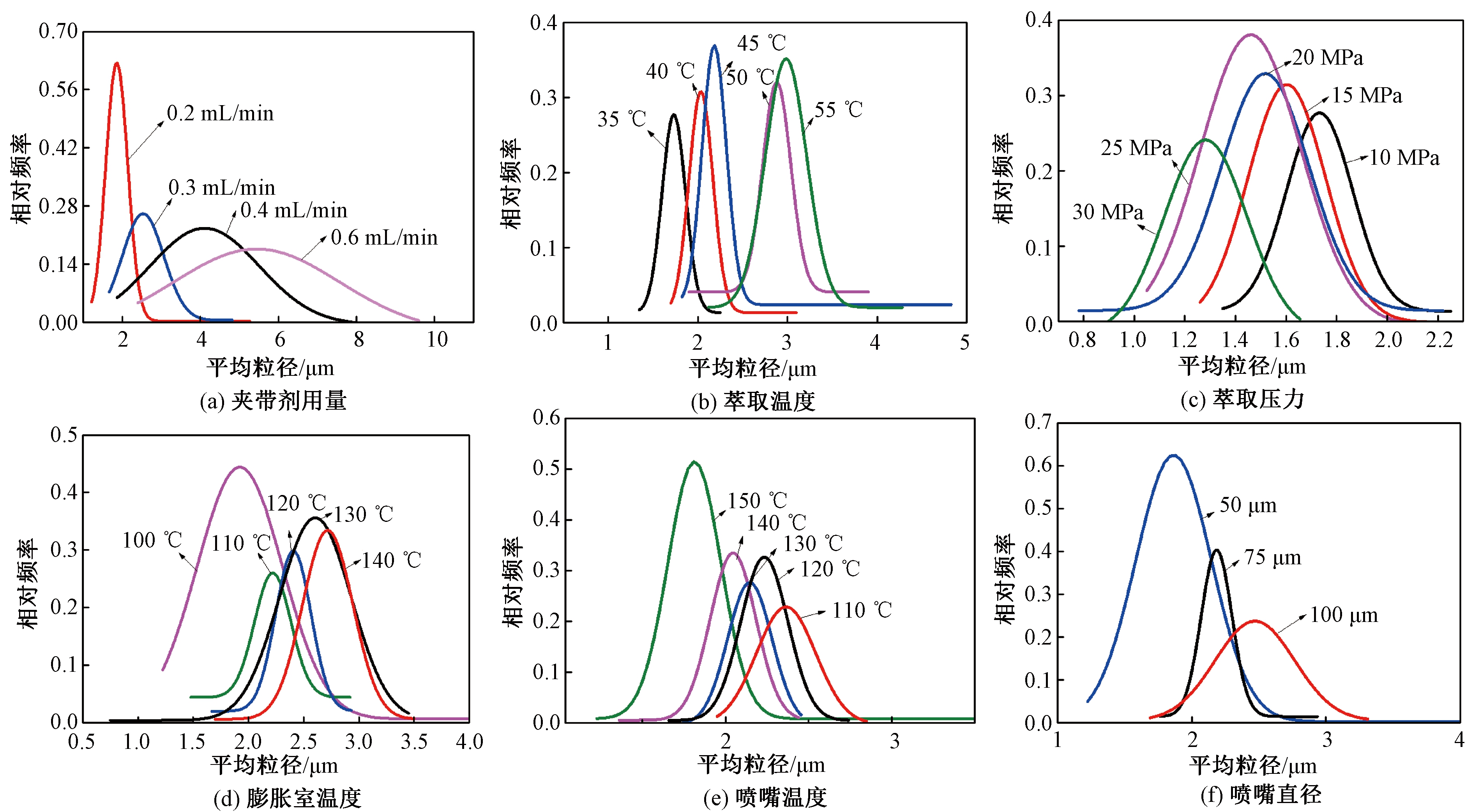
图2 不同夹带剂用量、萃取温度、萃取压力、膨胀室温度、喷嘴温度和喷嘴直径的微粒粒径分布
Fig.2 Particle size distribution under different of entrainer dosage, extraction temperature, extraction pressure,expansion chamber temperature, nozzle temperature and nozzle diameter
(4)膨胀室温度的影响.由图1(d)、图2(d)可知,FH 微粒粒径随着膨胀温度的升高而增大,平均粒径从100 ℃时的1.959 μm增加到了140 ℃时的2.726 μm.此外,图2(d)表明,随着膨胀室温度的升高,FH微粒的粒径分布范围开始变大.这是由于晶核形成之后,温度升高使收集釜中的晶体生长速度降低,晶体粒径增大.Helfgen[9]、Kayrak[10]、Shinozaki[11]等在使用RESS法制备微粒的研究中也得到了在较低膨胀室温度下微粒平均粒度较小的结论.因此,FH微粒制备可采用较低的膨胀室温度.
(5)喷嘴温度的影响.由图1(e)、图2(e)可知,随着喷嘴温度的升高,FH平均粒径随着温度的升高而降低,在110~150 ℃,平均粒径从2.378 μm降低到了1.959 μm.这是由于随着喷嘴温度的升高,FH在喷嘴处的过饱和度提高,膨胀过程中成核变多,因此得到的微粒粒径减小.因此,在较低的喷嘴温度下收集FH微粒更有利.
(6)喷嘴直径的影响.由图1(f)、图2(f)可知,喷嘴的直径为50 μm时,平均粒径为1.959 μm,喷嘴直径为100 μm时,平均粒径为2.610 μm.这是由于喷嘴直径越小时,溶液的过饱和度越大,膨胀时的速率越高,容易产生大量晶核,因此微粒粒径比较小;随着喷嘴直径的增大,溶液的膨胀速率降低,产生的晶核在喷嘴内停留时间增加,晶体生长时间增加,晶体的粒径会增大,也会发生团聚.因此,采用直径较小的喷嘴更容易获得粒径较小且分布均匀的FH药物微粒.
2.2 RESS制备FH微粒的正交实验结果
在设定膨胀室温度为100 ℃,喷嘴直径为50 μm的实验条件下,设计了四因素三水平正交实验,结果见表1.用极差法分析,在实验范围内以FH微粒平均粒径为主要评价指标,各因素的极差值R的大小为RC<RA<RD<RB,故各因素对FH微粒平均粒径的影响从小到大依次为C
2.3 FH原料及其微粒的表征
(1)FH的外貌型态.为观察FH微粒的外貌形态采用SEM分别对原料和RESS法得到的微粒进行了表征.由图3(a)可以看出,FH原料呈片状、棒状,长度约100 μm,宽度约10 μm,且尺寸分布极不均匀.图3(b)、(c)可知,得到的FH微粒呈球型或类球型的颗粒状微粒,微粒尺寸显著降低,且粒径分布比较均匀.图3(d)为较高的膨胀室温度下得到的微粒形态,出现少许的棒状结构,但与原料相比,尺寸也显著降低,长约10 μm,宽约1 μm.
(2)FH的FT-IR表征.图4(a)为原料FH和RESS后的FH的FT-IR结果,RESS前后的红外吸收光谱没有显著变化,未出现新的特征吸收峰,仅仅是吸收强度有所降低,结果表明,RESS前后FH并没有发生化学反应,即FH的化学结构保持不变.

图3 FH和FH经RESS后的SEM图
Fig.3 The SEM of FH raw materials and microparticles of FH
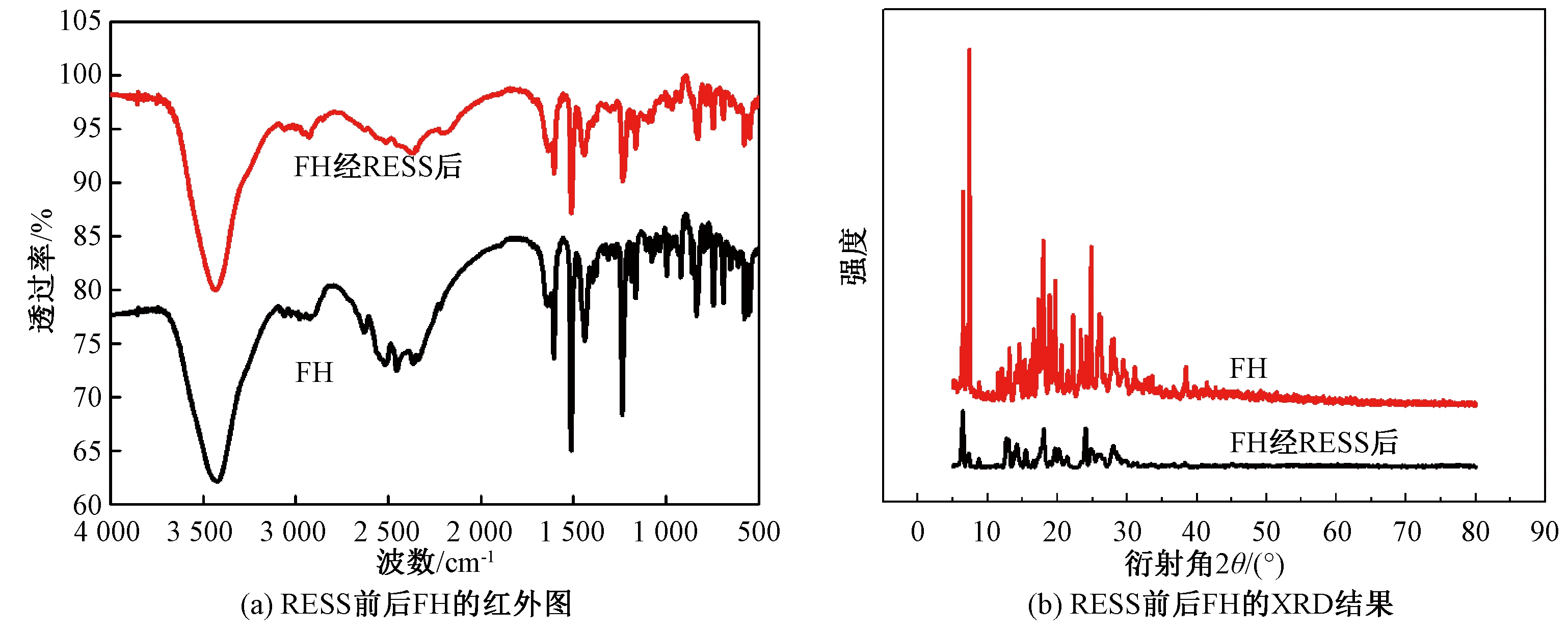
图4 RESS前后FH的红外图和XRD结果
Fig.4 FT-IR spectra and XRD patterns of FH original material and precipitated by RESS
(3)FH晶体行为的表征.FH微粒的结晶度可以通过XRD进行分析,图4(b)为FH原料和微粒的XRD图,结果表明在RESS前后FH具有相同的结构特征,但是,RESS得到的微粒的吸收强度相对于原料略有降低,这与文献[12]报道的结果是一致的,强度降低是由于RESS得到的微粒结晶度降低,微粒尺寸减小.
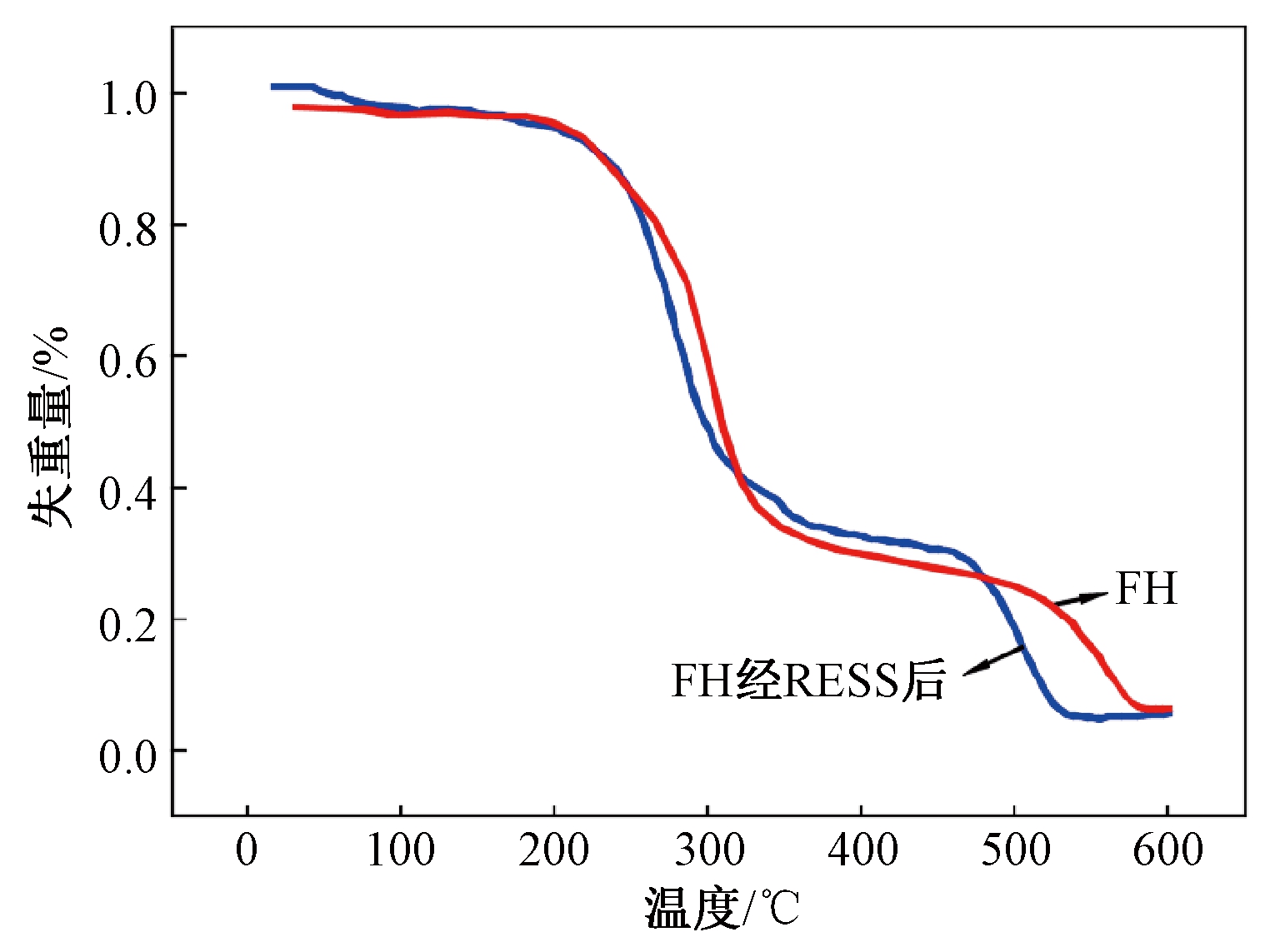
图5 FH和FH经RESS后的热重图
Fig.5 TGA scans of FH and FH processed by RESS
(4)FH的TGA表征.为了分析RESS前后FH的热稳定性变化,进行了热重分析.由图5可知,FH原料与微粒的两个样品的TGA稍有不同,但变化并不明显.
3 结论
(1)制备的FH微粒的平均粒径随夹带剂用量、萃取温度、膨胀室温度的增加而增加,随萃取压力、喷嘴温度的增加而降低.
(2)RESS制备的FH微粒平均粒径最大为6.893 μm,最小为1.285 μm,正交实验优化后最优组合为A1B2C2D2,即萃取温度为35 ℃,萃取压力为25 MPa,喷嘴温度140 ℃,夹带剂用量0.3 mL/min,此条件下微粒平均粒径为1.386 μm.
(3)为了考察RESS对FH的影响,采用FT-IR、XRD、TGA对FH原料及微粒进行表征,结果表明RESS前后FH的物理化学性质以及晶体结构保持稳定.
[1] 袁庆,刘得龙,余力生,等.氟桂利嗪预防性治疗前庭性偏头痛眩晕发作的前瞻性随机对照研究[J].临床耳鼻咽喉头颈外科杂志,2016,30(10):805-810.
[2] 张卫军.眩晕宁薄膜衣片与盐酸氟桂利嗦胶囊治疗系统性眩晕的临床对照[J].中国医院药学杂志,2011,31(13):1110-1112.
[3] YUN J H,LEE H Y,ASADUZZAMAN A K M,et al.Micronization and characterization of squid lecithin/polyethylene glycol composite using particles from gas saturated solutions (PGSS)process [J].Journal of industrial & engineering chemistry, 2013, 19(2):686-691.
[4] CHAROENCHAITRAKOOL M, F.DEHGHANI A, FOSTER N R, et al.Micronization by rapid expansion of supercritical solutions to enhance the dissolution rates of poorly water-soluble pharmaceuticals [J].Industrial & engineering chemistry research, 2000, 39(12):4794-4802.
[5] 陈琪, 裴占柱, 谢帮海,等.超临界溶液快速溶胀法制备醋酸泼尼松微粒[J].中国医药工业杂志, 2013, 44(12):1245-1248.
[6] YIM J H, KIM W S, LIM J S.Recrystallization of adefovir dipivoxil particles using the rapid expansion of supercritical solutions (RESS)process[J].Journal of supercritical fluids,2013,82:168-176.
[7] BASERI H, LOTFOLLAHI M N.Formation of gemfibrozil with narrow particle size distribution via rapid expansion of supercritical solution process (RESS)[J].Powder Technology, 2013, 235:677-684.
[8] TURK M,LIETZOW R.Formation and stabilization of submicron particles via rapid expansion processes[J].Journal of supercritical fluids, 2008,45(3):346-355.
[9] HELFGEN B, TURK M, SCHABER K.Theoretical and experimental investigations of the micronization of organic solids by rapid expansion of supercritical solutions[J].Powder technology, 2000, 110(1/2):22-28.
[10] KAYRAK D, AKMAN U, ÖNER H.Micronization of ibuprofen by RESS[J].Journal of supercritical fluids, 2003, 26(1):17-31.
[11] SHINOZAKI H, OGUCHI T, SUZUKI S, et al.Micronization and polymorphic conversion of tolbutamide and barbital by rapid expansion of supercritical solutions[J].Drug development & industrial pharmacy, 2006, 32(7):877-891.
[12] MONTES A, BENDEL A, KURTI R, et al.Processing naproxen with supercritical CO2[J].Journal of supercritical fluids, 2013, 75:21-29.